Page 58 - 《中国药房》2025年12期
P. 58
的相关结果可扫描本文首页二维码链接页面中“增强出 可减轻乳腺癌小鼠体内的炎症反应,抑制肿瘤细胞的生
[14]
版”板块查看附图3),与空白对照组相比,游离EMD组、 长和肺转移 。然而,该成分的生物利用度较低,故其
[6]
MWCNTs-EMD 组、HA-MWCNTs-EMD 组凋亡细胞有 在抗癌领域的应用前景有限 。研究表明,通过结构修
所增多,其凋亡率、LDH 释放量均显著升高(P<0.05); 饰或构建纳米载体系统可有效克服 EMD 这一缺陷,进
[6]
与游离EMD组相比,MWCNTs-EMD组、HA-MWCNTs- 而提升其抗癌活性 。CNTs 是常用于构建递药系统的
EMD组凋亡细胞亦有所增多,凋亡率、LDH释放量亦显 纳米材料,具有良好的细胞膜穿透性,可通过化学键合
著 升 高(P<0.05);与 MWCNTs-EMD 组 相 比 ,HA- 或者物理封装的方式包载穿透性较差的药物,并将其送
[15]
MWCNTs-EMD 组凋亡细胞亦有所增多,凋亡率、LDH 入目的细胞内,以提升药物的生物利用度 。Mumtaz
[16]
释放量亦显著升高(P<0.05)。 等 通过纳米技术构建了一种新型递药系统,可将喜树
碱、姜黄素、芦荟大黄素等天然成分输送到实验动物大
空白对照组 脑内的特定部位,进而增强其对胶质母细胞瘤的抑制作
用。本研究以氨基化 MWCNTs 为载体,制备了负载
EMD 的新型递药系统 MWCNTs-EMD。相关体外释药
和细胞摄取实验结果显示,与游离EMD相比,该递药系
游离EMD组 统可明显降低药物的24 h累积释放量,并可显著提高两
种乳腺癌细胞(MCF-7、MDA-MB-231细胞)对药物的摄
取量,表明 MWCNTs-EMD 具有一定的缓释作用,并能
MWCNTs-EMD组 提高靶向至乳腺癌细胞的EMD递送量。进一步的细胞
活力、凋亡、LDH 释放量检测结果显示,游离 EMD 和
MWCNTs-EMD 均可显著降低两种乳腺癌细胞的活力,
HA-MWCNTs-EMD组 显著升高其凋亡率和LDH释放量,表明两者均可有效抑
制乳腺癌细胞的增殖,诱导其凋亡并增加乳腺癌预后指
标LDH的释放。同时,本研究结果还表明,相较于游离
TUNEL DAPI 合并 EMD,MWCNTs-EMD 对乳腺癌细胞的抑制作用更强,
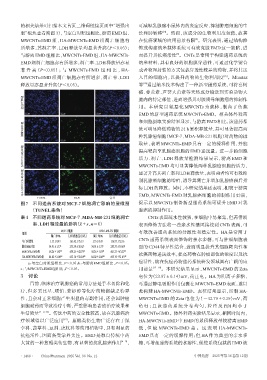
图7 不同递药系统对 MCF-7 细胞凋亡影响的显微图 提示以 MWCNTs 制备新型递药系统可提升 EMD 对乳
(TUNEL染色) 腺癌的抑制作用。
表4 不同递药系统对MCF-7、MDA-MB-231细胞凋亡 CNTs表面疏水性较强,在细胞中易聚集,但若借助
率、LDH释放量的影响(x±s,n=6) 表面修饰方法将一些亲水性基团接枝到 CNTs 表面,可
MCF-7细胞 MDA-MB-231细胞 有效改善递药系统的分散性和稳定性。HA 是常用于
组别
凋亡率/% LDH释放量/(U/L) 凋亡率/% LDH释放量/(U/L)
空白对照组 1.35±0.43 161.42±35.13 1.35±0.43 156.93±32.16 CNTs 递药系统表面修饰的亲水多糖,可与肿瘤细胞表
游离EMD组 34.91±1.37 a 275.39±38.62 a 34.91±1.37 a 283.37±39.60 a 面的 CD44 特异性结合,进而明显提升其细胞靶向性和
MWCNTs-EMD组 58.26±1.81 ab 439.25±42.73 ab 58.26±1.81 ab 461.21±43.27 ab 抗癌药物递送效率,提高药物在肿瘤部位的浓度以及抗
HA-MWCNTs-EMD组 84.02±2.06 abc 635.16±50.24 abc 84.02±2.06 abc 695.19±51.43 abc
a:与空白对照组相比,P<0.05;b:与游离EMD组相比,P<0.05; 癌活性,故在抗癌药物递药系统研发领域具有广阔的应
c:与MWCNTs-EMD组相比,P<0.05。 用前景 [17―18] 。本研究结果显示,MWCNTs-EMD 的 Zeta
3 讨论 电位为(23.87±0.14)mV,荷正电。HA 为阴离子多糖,
目前,临床治疗乳腺癌的常用方法是手术切除和化 可通过静电吸附作用包裹在MWCNTs-EMD表面,遂以
疗,但多柔比星、顺铂、紫杉醇等化疗药物都缺乏特异 此构建 HA-MWCNTs-EMD。表征结果显示,所制 HA-
性,且会对正常细胞产生明显的毒副作用,还会因肿瘤 MWCNTs-EMD 的 Zeta 电位为(-42.79±0.39)mV,荷
细胞耐药而导致治疗中断,严重影响患者的治疗效果和 负电 ;且该递药系统分布均匀,粒径及 PDI 均小于
生活质量 [1―2,12] 。传统中药的安全性较高,故在乳腺癌治 MWCNTs-EMD。体外释药实验结果显示,相同时间内,
[13]
疗领域得以广泛应用 。蒽醌类衍生物广泛存在于鼠 HA-MWCNTs-EMD 中 EMD 的累积释放量较游离 EMD
李科、茜草科、豆科、虎杖科等药用植物中,具有明显的 低 ,但 较 MWCNTs-EMD 高 。 这 表 明 HA-MWCNTs-
抗癌活性,因而备受学界关注。EMD 是源自传统中药 EMD 具有一定的缓释作用;但 HA 作为典型的亲水多
大黄的一种蒽醌类衍生物,有显著的抗乳腺癌作用 [4―5] , 糖,可增加递药系统的水溶性,促使系统包载的EMD被
· 1468 · China Pharmacy 2025 Vol. 36 No. 12 中国药房 2025年第36卷第12期