Page 88 - 《中国药房》2025年7期
P. 88
他滨组方案相对于支持治疗组方案的ICER为113 899.80 100
元/QALY;而采用吉西他滨组AEs处理成本上限(1 877.20 75
元)时,ICER 为 87 426.80 元/QALY,均小于本研究设定 支持治疗组
吉西他滨组
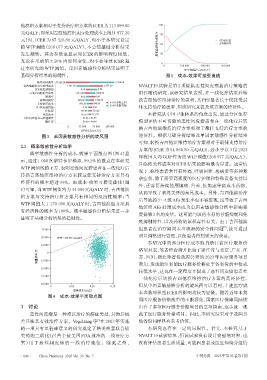
的 WTP 阈值(268 077 元/QALY),不会使基础分析结果 具有经济性的概率/% 50
发生翻转。其余参数也显示对 ICER 的影响程度较低, 25
无论在基础值±20% 内如何变化,均不会导致 ICER 超
0
过本研究的WTP阈值。单因素敏感性分析结果证明了 0 150 000 300 000 450 000
WTP阈值/(元/QALY)
基础分析结果的稳健性。 图5 成本-效果可接受曲线
临终关怀成本 17 245.20 11 496.80
吉西他滨组AEs处理成本 1 251.40 1 877.20 NVALT19 试验是第 2 项提供恶性间皮瘤新治疗策略的
PFS状态效用值 0.78 0.52
二线(PD期)治疗成本 3 012.90 2 008.60 阳性随机研究,该研究结果表明,在一线化疗结束后转
贴现率 0.03 0.08
检查检验费 885.60 1 328.40 换吉西他滨维持治疗的患者,其PFS显著长于仅接受最
支持治疗成本 660.10 990.20 ICER(参数上浮)
PD状态效用值 0.38 0.56 ICER(参数下降) 佳支持治疗的患者,但该研究未提及该方案的经济性。
住院费 492.80 739.20
药品成本 142.50 213.70 本研究从中国卫生体系的角度出发,通过分区生存
支持治疗组AEs处理成本 92.60 61.70
输注费 59.90 89.90 模型评估不可切除的恶性间皮瘤患者在一线化疗后转
0 35 000 70 000 105 000 换吉西他滨维持治疗方案相对于最佳支持治疗方案的
ICER/(元/QALY)
图3 单因素敏感性分析的旋风图 经济性。根据基础分析结果及单因素敏感性分析结果
可知,转换吉西他滨维持治疗方案相对于最佳支持治疗
2.3 概率敏感性分析结果
方案的 ICER 为 54 860.50 元/QALY,远小于以 3 倍 2023
概率敏感性分析的成本-效果平面散点图(图 4)显
年我国人均GDP作为的WTP阈值(268 077元/QALY),
示,通过 1 000 次蒙特卡罗模拟,99.2% 的散点在本研究
且临终关怀成本对ICER结果的影响最为显著。通常情
WTP阈值线的下方,表明恶性间皮瘤患者在一线化疗后
况下,临终患者常伴有疼痛、呼吸困难、恶病质等多种复
转换吉西他滨维持治疗方案较最佳支持治疗方案具有
杂症状,除了需要高强度的医疗护理和特殊设备支持以
经济性的概率超过 99%。由成本-效果可接受曲线(图
外,还需要持续使用镇痛、营养、抗焦虑等高成本药物,
5)可知,当WTP阈值约为44 000元/QALY时,吉西他滨
从而导致了临终关怀的高昂成本。另外,吉西他滨治疗
组方案与支持治疗组方案具有相同的经济性概率;当
后导致的3~4级AEs发生率也不容忽视,这导致了吉西
WTP 阈值大于 270 000 元/QALY 时,吉西他滨组方案具
他滨组 AEs 处理成本成为单因素敏感性分析中影响程
有经济性的概率为100%。概率敏感性分析结果进一步
度排第2名的变量。这可能与该药本身的骨髓抑制和免
证明了基础分析结果的稳健性。
疫抑制特性,以及药物的累积毒性有关。由于吉西他滨
[7]
37 500 组患者在治疗期间未出现新的安全性问题 ,故可通过
剂量调整进行管理,以使患者得到更大的获益。
25 000 WTP=268 077元/QALY
本研究中的部分医疗成本取自浙江省医疗服务价
12 500 格项目表,笔者经查询并比较了浙江省与北京、广东、江
增量成本/元 -12 500 0 苏、四川、湖北等省份政府公开的 2023 年医疗服务项目
-25 000 费用,发现浙江省的医疗服务价格处于各省份的中位或
较低水平,这也在一定程度上促成了恶性间皮瘤患者在
-37 500
一线化疗后转换吉西他滨维持治疗方案的高经济性。
-50 000
0 0.05 0.10 0.15 但从单因素敏感性分析的旋风图可以看到,上述医疗成
增量效果/QALY 本参数对模型ICER的影响均较为轻微。随着近年来我
图4 成本-效果平面散点图
国医疗服务价格改革的不断深化,国家医疗保障局陆续
3 讨论 出台了多项医疗服务价格项目的立项指南,逐步统一规
恶性间皮瘤是一种难以治疗的癌症类型,其预后极 范了医疗服务价格项目。因此,本研究结果对于我国其
差且缺乏有效治疗方案。Vogelzang 等 在 2003 年实施 他省份同样具有参考价值。
[5]
的一项具有里程碑意义的研究奠定了培美曲塞联合铂 本研究也存在一定的局限性。首先,本研究基于
类药物二联化疗(首个被美国 FDA 批准的一线治疗方 NVALT19 试验结果,但该试验没有设计安慰剂对照,也
案)用于恶性间皮瘤的一线治疗地位。除此之外, 没有评估患者生活质量,可能因患者或医生知晓分组情
· 846 · China Pharmacy 2025 Vol. 36 No. 7 中国药房 2025年第36卷第7期