Page 46 - 《中国药房》2022年5期
P. 46
4 a
1.5
a
空白对照组
a a
莪术醇12.5 μg/mL组 a a
3
莪术醇25 μg/mL组 1.0
mRNA表达水平 2 莪术醇100 μg/mL组 ROS水平 0.5
莪术醇50 μg/mL组
1 a a
a a
a a a a
0
0 空白对 莪术醇12.5 莪术醇25 莪术醇33 莪术醇50 莪术醇100
μg/mL组
μg/mL组
μg/mL组 μg/mL组 μg/mL组
照组
p21 PCNA CDK2
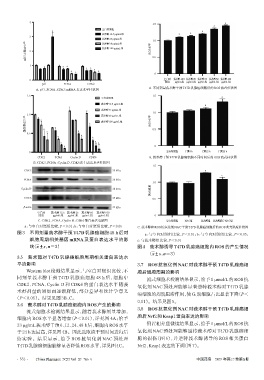
A. 不同剂量莪术醇干预T47D乳腺癌细胞后的ROS流式柱状图
A. p21、PCNA、CDK2 mRNA表达水平柱状图
1.5 1.5 a
空白对照组
莪术醇12.5 μg/mL组
b
莪术醇25 μg/mL组
1.0
1.0 莪术醇50 μg/mL组
蛋白表达水平 a b b 莪术醇100 μg/mL组 ROS水平
0.5 a a b 0.5
a a
b
a
a a
a 0
0 空白对照组 干预6 h 干预12 h 干预24 h
CDK2 PCNA Cyclin D CDK6 B. 莪术醇干预T47D乳腺癌细胞不同时间后的ROS流式柱状图
B. CDK2、PCNA、Cyclin D、CDK6蛋白表达水平柱状图
1.5
CDK2 33 kDa a
c
PCNA 36 kDa
1.0
荧光强度
Cyclin D 36 kDa
CDK6 37 kDa 0.5
β-actin 42 kDa
空白对 莪术醇12.5 莪术醇25 莪术醇50 莪术醇100
照组 μg/mL组 μg/mL组 μg/mL组 μg/mL组 0
C. CDK2、PCNA、Cyclin D、CDK6蛋白表达电泳图 空白对照组 NAC组 莪术醇组 莪术醇联合NAC组
a:与空白对照组比较,P<0.01;b:与空白对照组比较,P<0.05 C. 莪术醇和ROS抗氧化剂NAC干预T47D乳腺癌细胞后的ROS荧光强度柱状图
图 3 不同剂量莪术醇干预 T47D 乳腺癌细胞 48 h 后对 a:与空白对照组比较,P<0.01;b:与空白对照组比较,P<0.05;
细胞周期相关基因 mRNA 及蛋白表达水平的影 c:与莪术醇组比较,P<0.01
响(x±±s,n=3) 图4 莪术醇诱导T47D乳腺癌细胞内ROS的产生情况
(x±±s,n=3)
3.5 莪术醇对 T47D 乳腺癌细胞周期相关蛋白表达水
平的影响 3.7 ROS抗氧化剂NAC对莪术醇干预T47D乳腺癌细
Western blot 检测结果显示,与空白对照组比较,不 胞后细胞周期的影响
同剂量莪术醇干预 T47D 乳腺癌细胞 48 h 后,细胞中 流式细胞术检测结果显示,给予1 μmol/L的ROS抗
CDK2、PCNA、Cyclin D 和 CDK6 的蛋白表达水平随莪
氧化剂 NAC 预处理能够显著逆转莪术醇对 T47D 乳腺
术醇剂量的增加而逐渐降低,部分差异有统计学意义
癌细胞的周期阻滞作用,使G1期细胞占比显著下降(P<
(P<0.05)。结果见图3B、C。
3.6 莪术醇对T47D乳腺癌细胞内ROS产生的影响 0.01)。结果见图5。
3.8 ROS抗氧化剂NAC对莪术醇干预T47D乳腺癌细
流式细胞术检测结果显示,随着莪术醇剂量增加,
胞后Nrf2和Keap1蛋白表达的影响
细胞内 ROS 水平显著增加(P<0.01),详见图 4A;给予
33 μg/mL莪术醇干预6、12、24、48 h后,细胞内ROS水平 倒置相差显微镜结果显示,给予1 μmol/L的ROS抗
于24 h达最高,详见图4B。因此选取该干预时间进行后 氧化剂 NAC 预处理能够逆转莪术醇对 T47D 乳腺癌细
续实验。结果显示,给予 ROS 抗氧化剂 NAC 预处理 胞的损伤(图 6),并逆转莪术醇诱导的 ROS 相关蛋白
T47D乳腺癌细胞能够显著降低ROS水平,详见图4C。 Nrf2、Keap1表达的下调(图7)。
·552 · China Pharmacy 2022 Vol. 33 No. 5 中国药房 2022年第33卷第5期