Page 84 - 2020年17期
P. 84
为纯净水(浙江娃哈哈集团有限公司,批号:20180407)。 紫丁香苷
50
表1 大接骨丹药材采集信息 40
30
Tab 1 Collection information of T. angulata mAU 20
10
0
不同用药部位编号 0 5 10 15 20 25
采集时间 t,min
根皮 树皮 叶
A.对照品溶液
2017-01-15 G1 S1 未采集
2017-02-15 G2 S2 未采集 80
2017-03-15 G3 S3 未采集 mAU 60
40
2017-04-15 G4 S4 Y4 20 紫丁香苷
0
2017-05-15 G5 S5 Y5 0 5 10 15 20 25
2017-06-15 G6 S6 Y6 t,min
2017-07-15 G7 S7 Y7 B.供试品溶液(样品编号:G1)
2017-08-15 G8 S8 Y8 16
2017-09-15 G9 S9 Y9 12
2017-10-15 G10 S10 Y10 mAU 8
4
2017-11-15 G11 S11 Y11 0
2017-12-15 G12 S12 Y12 0 5 10 15 20 25
t,min
2 方法与结果 C.空白对照
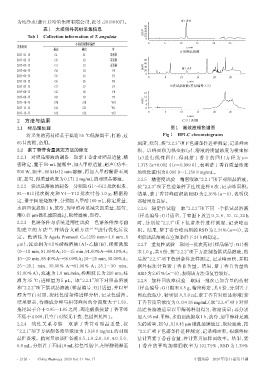
2.1 样品预处理 图1 高效液相色谱图
将采集的药材样品于烘箱55 ℃低温烘干,打粉,过 Fig 1 HPLC chromatograms
65目药筛,备用。 刻度,摇匀,按“2.2.3”项下色谱条件进样测定,记录峰面
2.2 紫丁香苷含量测定方法的建立 积。以峰面积为纵坐标(y)、溶液的质量浓度为横坐标
2.2.1 对照品溶液的制备 取紫丁香苷对照品适量,精 (x)进行线性回归,得到紫丁香苷的回归方程为 y=
密称定,置于50 mL量瓶中,加入甲醇适量,超声(功率: 1.375 3x+0.002 4(r=0.999 6),表明紫丁香苷质量浓度
500 W,频率:40 kHz)2 min 溶解,再加入甲醇稀释至刻 的线性范围为0.095 9~1.150 8 mg/mL。
度,摇匀,得质量浓度为0.171 2 mg/mL的对照品溶液。 2.2.5 精密度试验 精密吸取“2.2.1”项下对照品溶液,
2.2.2 供试品溶液的制备 分别取G1~G12批次根皮、 按“2.2.3”项下色谱条件下连续进样 6 次,记录峰面积。
S1~S12 批次树皮和 Y4~Y12 批次叶各 1.0 g,精密称 结果,紫丁香苷峰面积的 RSD 为 2.16%(n=6),表明仪
定,置于圆底烧瓶中,分别加入甲醇100 mL,称定质量, 器精密度良好。
水浴回流提取1 h,放冷,加甲醇补足减失的质量,摇匀, 2.2.6 稳定性试验 取“2.2.2”项下同一个供试品溶液
用0.45 μm微孔滤膜滤过,取续滤液,即得。 (样品编号:G1)适量,于室温下放置 0、2、6、10、12、24 h
2.2.3 色谱条件与系统适用性试验 色谱条件参考前 时,分别按“2.2.3”项下色谱条件进样测定,记录峰面
期建立的方法 ,并结合文献方法 [17-20] 进行优化后设 积。结果,紫丁香苷峰面积的 RSD 为 2.34%(n=6),表
[16]
定。色谱柱为 Agela Promosil C18 (250 mm×4.6 mm,5 明供试品溶液在室温条件下24 h内稳定。
μm);流动相为 0.5%磷酸溶液(A)-乙腈(B),梯度洗脱 2.2.7 重复性试验 取同一批次药材(样品编号:G1)粉
(0~10 min,91.00%A;10~15 min,91.00%A→88.40%A; 末1.0 g,共6份,按“2.2.2”项下方法制备供试品溶液,然
15~20 min,88.40%A→30.00%A;20~25 min,30.00%A; 后按“2.2.3”项下色谱条件进样测定,记录峰面积,并根
25~25.1 min,30.00% A→91.00% A;25.1~30 min, 据外标法计算紫丁香苷含量。结果,紫丁香苷含量的
91.00%A);流速为 1.0 mL/min;检测波长为 210 nm;柱 RSD为2.67%(n=6),表明该方法重复性较好。
温为 35 ℃;进样量为 5 μL。取“2.2.1”项下对照品溶液 2.2.8 加样回收率试验 取同一批次已知含量的药材
和“2.2.2”项下供试品溶液(样品编号:G1)适量,并以甲 (样品编号:G1)粉末 0.5 g,精密称定,共 6 份,分别置于
醇为空白对照,按此色谱条件进样分析,记录色谱图。 圆底烧瓶中,精密加入 5.0 mL 紫丁香苷对照品溶液[紫
结果显示,待测成分峰与相邻峰间的分离度大于 1.50、 丁香苷质量浓度为 0.134 26 mg/mL(取“2.2.4”项下对照
拖尾因子介于 0.95~1.05 之间,理论板数按紫丁香苷峰 品贮备溶液适量以甲醇稀释制得)],称定质量;再分别
不低于4 000,且空白对照无干扰,色谱图见图1。 加入95 mL甲醇,水浴回流提取1 h,放冷,加甲醇补足减
2.2.4 线性关系考察 取紫丁香苷对照品适量,按 失的质量,摇匀,用0.45 μm微孔滤膜滤过,取续滤液,按
“2.2.1”项下方法制备质量浓度为1.918 0 mg/mL的对照 “2.2.3”项下色谱条件进样测定,记录峰面积,根据外标
品贮备液。精密量取该贮备液0.5、1.0、2.0、3.0、4.0、5.0、 法计算紫丁香苷含量,并计算其加样回收率。结果,紫
6.0 mL,分别置于不同10 mL棕色量瓶中,用甲醇稀释至 丁香苷的平均加样回收率为 101.74%,RSD 为 1.39%
·2126 · China Pharmacy 2020 Vol. 31 No. 17 中国药房 2020年第31卷第17期