Page 92 - 《中国药房》2024年1期
P. 92
ceiver operating characteristic curve,ROC)中的约登指数 表1 rs1801133 位点基因型、MTX 给药剂量及其 24 h
预测不良反应影响因素的阈值。 血药浓度与不良反应的单因素分析结果
2 结果 rs1801133位点基因型 MTX给药剂量 MTX 24 h血药浓度
不良反应 C等位基因 T等位基因
2.1 临床资料 P (x±s)/(g/m) P [M(Q 1,Q 3)]/(μmol/L) P
2
占比/% 占比/%
我院骨科2020年6月至2022年10月共收治了53例 肝功能损害 57.6 55.3 0.812 7.51±1.03 0.974 3.73(1.81,7.76) 0.001
首次入院进行HD-MTX单药治疗的骨肉瘤患者,其中男 肾功能损害 3.4 12.8 0.148 7.81±0.63 0.561 40.00(11.74,70.32) 0.000 03
血液学毒性 8.5 27.7 0.009 7.57±1.19 0.858 3.66(1.425,13.65) 0.346
性 37 例、女性 16 例;平均年龄(15.13±6.51)岁;平均身
胃肠道反应 96.6 91.5 0.477 7.51±1.07 0.824 2.55(1.5,7.28) 0.229
高(161.57±17.79) cm;平均体重(52.03±18.23) kg;平
2.5 HD-MTX致不良反应的相关因素分析
2
均用药剂量(7.51±1.04) g/m 。
根据上述单因素分析结果,对 rs1801133 位点基因
2.2 基因分型结果
型与血液学毒性的不良反应进行二元 Logistic 回归分
53例患者中,共检出CC野生型16例、CT杂合型27
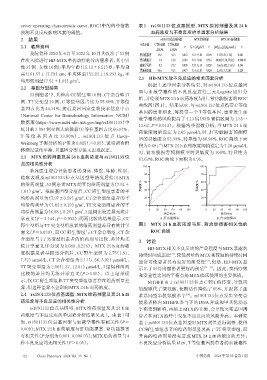
析,并绘制MTX 24 h血药浓度与肝、肾功能损害的ROC
例、TT 突变型 10 例,C 等位基因占比为 55.66%,T 等位
曲线图(图1)。结果显示,与rs1801133位点携带C等位
基因占比为 44.34%,接近美国国家生物技术信息中心
基因的患者相比,每携带一个 T 等位基因,患者发生血
(National Center for Biotechnology Information,NCBI)
液学毒性的风险提高了 4.13 倍(95% 置信区间为 1.35~
数据库(https://www.ncbi.nlm.nih.gov/snp/rs1801133)中
12.62,P=0.013)。根据约登指数分析,当 MTX 24 h 血
统计的3 984例亚洲人的数据(C等位基因占比66.14%、
药浓度阈值设定为 2.65 μmol/L 时,肝功能损害预测模
T 等 位 基 因 占 比 33.86%)。 rs1801133 位 点 Hardy-
型的灵敏度为53.33%,特异性为86.96%,ROC曲线下面
Weinberg平衡分析的P值为0.815(>0.05),说明调查群
积为0.69;当MTX 24 h血药浓度阈值设定为7.28 μmol/L
体满足遗传平衡,且基因分型方法未出现误差。
时,肾功能损害预测模型的灵敏度为 100%,特异性为
2.3 MTX 给药剂量及其 24 h 血药浓度与 rs1801133 位
81.63%,ROC曲线下面积为0.95。
点的相关性分析
100 100
临床医生综合评估患者的身高、体重、年龄、性别、
80 80
临床表现及 rs1801133 位点基因型等情况后给出 MTX
的给药剂量,53例患者MTX的平均给药剂量为(7.51± 灵敏度/% 60 灵敏度/% 60
2
1.04) g/m 。根据基因型分组后,CC 野生型组患者的平 40 40
2
均给药剂量为(7.97±0.29) g/m ,CT杂合型组患者的平 20 20
2
均给药剂量为(7.44±0.19) g/m ,TT突变型组患者的平 0 0
2
均给药剂量为(6.98±0.25) g/m ,3组间比较差异无统计 0 20 40 60 80 100 0 20 40 60 80 100
特异性/% 特异性/%
学意义(F=3.144,P=0.052);两两比较的结果显示,CC A.肝功能损害 B.肾功能损害
野生型组与TT突变型组患者的给药剂量差异有统计学 图1 MTX 24 h 血药浓度与肝、肾功能损害相关性的
意义(P=0.030),而CC野生型组与CT杂合型组、CT杂 ROC曲线
合型组与 TT 突变型组患者的给药剂量比较,差异均无
3 讨论
统计学意义(P 分别为 0.080、0.276)。MTX 24 h 血药浓
HD-MTX相关不良反应的严重程度与MTX暴露的
度根据患者基因型分组后,CC 野生型组为 2.75(1.81, [11]
持续时间成正比 ,较低剂量的MTX和较短的持续时间
7.32) μmol/L,CT 杂合型组为 2.11(1.24,3.92) μmol/L, [12]
通常可使患者具有良好的耐受性 ;但是,HD-MTX 显
TT 突变型组为 2.56(1.37,12.01) μmol/L,3 组间和两两 [13―14]
示出了对骨肉瘤患者更好的预后 。因此,找到疗效
比较的差异均无统计学意义(P>0.05)。以上结果提 和安全性之间的平衡点是MTX临床使用的主要挑战。
示,仅CC野生型组和TT突变型组患者存在给药剂量差 MTHFR 由于 rs1801133 位点 C 到 T 的转变,导致丙
异,但这种差异不会影响MTX 24 h 血药浓度。 氨酸取代了缬氨酸,使酶活性降低了 65%,并提高了血
2.4 rs1801133位点基因型、MTX给药剂量及其24 h血 浆总同型半胱氨酸水平 。rs1801133 位点发生突变会
[15]
药浓度与不良反应的相关性分析 使患者体内 MTHFR 参与下的 DNA 合成和甲基化动态
rs1801133 位点基因型、MTX 给药剂量及其 24 h 血 平衡受到影响,再加上MTX的干预,会导致突变基因携
药浓度与不良反应的单因素分析结果见表1。由表1可 带者在MTX治疗中发生不良反应的风险升高。本研究
知,rs1801133 位点基因型与血液学毒性有相关性(P= 基于rs1801133位点基因型对MTX剂量进行调整,使得
0.009);MTX 24 h 血药浓度与肝功能损害、肾功能损害 CC野生型组患者的给药剂量显著高于TT突变型组,而
有相关性(P分别为0.001、0.000 03);MTX给药剂量与4 升高的给药剂量没有造成 MTX 24 h 血药浓度的差异;
种不良反应均无相关性(P>0.05)。 不良反应分析结果显示,T等位基因携带者的血液毒性
· 82 · China Pharmacy 2024 Vol. 35 No. 1 中国药房 2024年第35卷第1期