Page 94 - 《中国药房》2023年18期
P. 94
Meta-analysis estimates,given named study is omitted 0
Lower CI Limit Estimate Upper CI Limit
Martinez arm A (2021)
Martinez arm B (2021) 0.5
Rodriguez-moreno (2020)
Gao (2020)
Van dijk (2020)
Necchi (2020) ( log[OR] )
Powles (2019) 1.0
Gupta (2022)
Cathomas (2020)
Galsky (2021) SE
Rose (2021)
Funt (2022) 1.5
Zhang (2022)
Natesan (2021)
Wei (2020)
Goubet (2022)
Guercio armA (2022) 2.0
Guercio armB (2022)
Grivas armA (2021) 0.001 0.1 1.0 10 100
Grivas armB (2021) OR
Kim (2022)
Xing (2021)
Grande armA (2022) A.pCR率
Thibault (2020)
Lin (2022)
Van dorp (2021) 0
Kaimakliotis (2020)
Necchi (2022)
0.5
-0.68 -0.64 -0.42 -0.19 -0.15
A. pCR率 ( log[OR] ) 1.0
Meta-analysis estimates,given named study is omitted SE
1.5
Lower CI Limit Estimate Upper CI Limit
Gao (2020)
Van dijk (2020) 2.0
Necchi (2020)
Powles (2019) 0.001 0.1 1.0 10 100
Gupta (2022) OR
Cathomas (2020) B. Grade≥3 irAEs发生率
Galsky (2021)
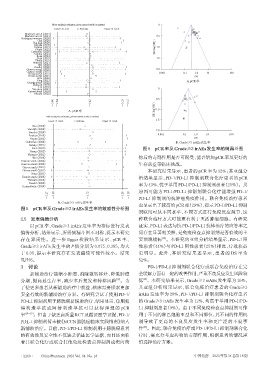
Funt (2022) 图6 pCR率及Grade≥≥3 irAEs发生率的倒漏斗图
Zhang (2022)
Natesan (2021)
Wei (2020) 物后的毒副作用是否可耐受,能否增加pCR率及更好的
Guercio armA (2022)
Guercio armB (2022) 生存获益等临床挑战。
Grivas armA (2021)
Grivas armB (2021) 本研究结果显示,患者的 pCR 率为 32%;其亚组分
Xing (2021)
Grande armA (2020) 析结果显示,PD-1/PD-L1 抑制剂联合化疗患者的 pCR
Thibault (2020)
Necchi (2022) 率为43%,优于单用PD-1/PD-L1抑制剂患者(25%)。其
Kaimakliotis (2020)
原因可能为 PD-1/PD-L1 抑制剂联合化疗能增强 PD-1/
-2.27 -2.19 -1.72 -1.26 -1.18 PD-L1 抑制剂的抗肿瘤免疫作用。联合免疫治疗患者
B. Grade≥3 irAEs发生率 也显示出了较高的pCR率(29%),提示PD-1/PD-L1抑制
图5 pCR率及Grade≥≥3 irAEs发生率的敏感性分析图
剂联用可从不同水平、不同方式进行免疫反应调节,这
2.5 发表偏倚分析 种联合治疗方式可能更有利于灭活肿瘤细胞。有研究
以 pCR 率、Grade≥3 irAEs 发生率为指标进行发表 证实,PD-L1表达与抗PD-1/PD-L1抗体治疗的应答率之
偏倚分析,结果显示,所得倒漏斗图不对称,提示本研究 间存在显著相关性,是免疫检查点抑制剂是否有效的主
[38]
存在异质性。进一步 Egger 检验结果显示,pCR 率、 要预测指标 。本研究的亚组分析结果显示,PD-L1 阳
Grade≥3 irAEs 发生率的 P 值分别为 0.075、0.385,均大 性患者(44%)与 PD-L1 阴性患者(25%)相比,疗效获益
于 0.05,提示本研究存在发表偏倚可能性较小。结果 更明显。此外,本研究结果还显示,患者的 DS 率为
见图6。 52%。
3 讨论 PD-1/PD-L1 抑制剂联合化疗或联合免疫治疗在完
新辅助治疗能缩小肿瘤、消除微转移灶、降低肿瘤 全缓解方面有一定的改善作用,严重不良反应发生风险较
[39]
[37]
分期,提高总生存率,减少术后复发和转移风险 。为 低 。本研究结果显示,Grade≥3 irAEs 发生率为 16%,
了使更多患者从新辅助治疗中获益,临床需要探索更加 其亚组分析结果显示,联合免疫治疗患者的 Grade≥3
安全有效的新辅助治疗方案。有研究尝试了使用PD-1/ irAEs 发生率为 28%,PD-1/PD-L1 抑制剂联合化疗患者
PD-L1抑制剂用于膀胱癌新辅助治疗,结果显示,单用帕 的 Grade≥3 irAEs 发生率为 12%,均高于单用 PD-1/PD-
博利珠单抗或阿替利珠单抗可以获得理想的 pCR L1抑制剂患者(9%)。由于不同免疫检查点抑制剂可作
率 [16―17] 。但由于缺乏高质量RCT及循证医学证据,PD-1/ 用于不同的淋巴细胞亚型和不同部位,其不同的作用机
PDL-1抑制剂暂未被《NCCN膀胱癌临床实践指南》纳入 制导致了更高的不良反应发生率和更广泛的不良事
[40]
新辅助治疗。目前,PD-1/PD-L1抑制剂用于膀胱癌患者 件 。因此,联合免疫治疗或PD-1/PD-L1抑制剂联合化
的有效性及安全性不仅缺乏循证医学证据,而且还面临 疗时,需充分考虑药物的毒副作用,根据患者的情况谨
着其联合化疗或联合其他免疫检查点抑制剂或靶向药 慎选择治疗方案。
· 2260 · China Pharmacy 2023 Vol. 34 No. 18 中国药房 2023年第34卷第18期