Page 30 - 《中国药房》2023年8期
P. 30
70 2 500 3.1 ATV 6.0×10 4 3.0 ATV
60
2 000 5.0×10 4 4
50
intensity/cps 40 intensity/cps 1 500 intensity/cps 4.0×10 4 4
3.0×10
30
1 000
20
500 2.0×10
10 1.0×10 4
0 0 0
0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0
t/min t/min t/min
3.2 3.1
30 ALT ALT
200 2 500
25 150 2 000
intensity/cps 15 intensity/cps 100 intensity/cps 1 500
20
1 000
10
5 50 500
0 0 0
0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0
t/min t/min t/min
40 2.9 2.9
2-HAT 2-HAT
4.0×10 4
1 500
30 3.0×10 4
intensity/cps 20 intensity/cps 1 000 intensity/cps 2.0×10 4
500
10
4
1.0×10
1.6 3.3 3.7
0 0 0
0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0
t/min t/min t/min
60 4-HAT 2 500 4-HAT
300
50 2 000
250 1.5 1.5
intensity/cps 30 intensity/cps 200 intensity/cps 1 500
40
150
1 000
20
10 100 500 1.8
50
0 0 0
0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0
t/min t/min t/min
1.3 1.3
80 PIV 3.5×10 4 PIV
2.5×10 4
3.0×10 4
60 2.0×10 4 2.5×10 4
intensity/cps 40 intensity/cps 1.5×10 4 4 intensity/cps 2.0×10 4 4
1.5×10
1.0×10
20 1.0×10 4
5 000 5 000
0 0 0 1.9 2.2
0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0
t/min t/min t/min
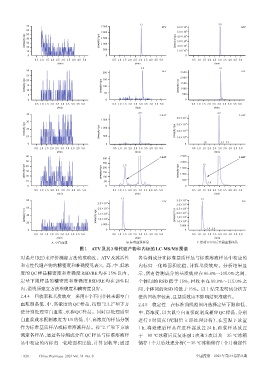
A.空白血浆 B.标准血浆样品 C.给药0.33 h后大鼠血浆样品
图1 ATV及其3种代谢产物和内标的LC-MS/MS图谱
对误差(RE)来评价测定方法的准确度。ATV及其活性 各待测成分在标准基质样品与标准溶液样品中相应的
和毒性代谢产物的精密度和准确度见表3。高、中、低浓 内标归一化峰面积比值,计算基质效应。分析结果显
度的 QC 样品精密度和准确度 RSD/RE 均在 15% 以内, 示,所有待测成分的基质效应在 86.8%~105.0% 之间,
定量下限样品的精密度和准确度 RSD/RE 均在 20% 以 个体间的 RSD 低于 15%;回收率在 88.0%~115.0% 之
内,说明所建立方法准确度和精密度良好。 间,个体间的RSD均低于15%。以上结果表明该分析方
2.4.4 回收率和基质效应 采用6个不同个体来源空白 法的回收率较高,且基质效应不影响结果准确性。
血浆制备低、中、高浓度的 QC 样品,按照“2.3.2”项下方 2.4.5 稳定性 在标准曲线范围内选择定量下限和低、
法分别处理空白血浆、水和 QC 样品。同时以处理后空 中、高浓度,以大鼠空白血浆配制成相应 QC 样品,分别
白血浆或水配制浓度为1/5的低、中、高浓度的样品分别 进行 0 时间点(配制后立即处理分析)、在室温下放置
作为标准基质样品或标准溶液样品。按“2.1”项下方法 1 h、将处理后样品在进样器放置 24 h、血浆样品放置
测定各样品,通过各待测成分在 QC 样品与标准溶液样 于-80 ℃冰箱后反复冻融 1 次和 3 次以及-35 ℃冰箱
品中相应的内标归一化峰面积比值,计算回收率;通过 储存1个月后处理分析(-35 ℃冰箱储存1个月稳定性
· 920 · China Pharmacy 2023 Vol. 34 No. 8 中国药房 2023年第34卷第8期