Page 24 - 《中国药房》2023年2期
P. 24
MXF低、中、高剂量组每个粪便样本中称取相同质量的 中剂量组小鼠第 3~5 天、MXF 高剂量组小鼠第 2~7 天
粪便样品,置于同一容器中,混合均匀,按照“2.4.1(2)” 体质量显著低于空白组(P<0.05)。与空白组相比,各
项下供试品溶液制备方法制备QC样本溶液。 给药组小鼠的肛温差异均无统计学意义。给药第2天,
2.4.2 色谱条件与质谱条件 (1)色谱条件:色谱柱为 MXF 中、高剂量组有小鼠死亡,生存率分别为 58.33%、
HALO-C18 (2.1 mm×100 mm,2.7 μm),以 0.05% 甲酸溶 50.00%,后续指标检测按代谢组学样本数量的最低要求
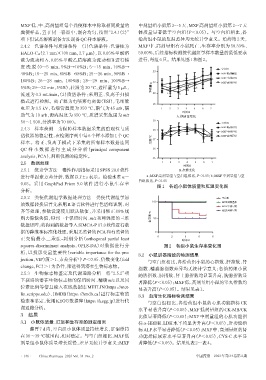
液为流动相 A、0.05% 甲酸乙腈溶液为流动相 B 进行梯 进行,每组6只。结果见图1和图2。
度 洗 脱(0~5 min,5%B→10%B;5~15 min,10%B→ 空白组
24
40%B;15~25 min,40%B→98%B;25~26 min,98%B→ MXF低剂量组
a a MXF中剂量组
100%B;26~28 min,100%B;28~29 min,100%B→ 22 a MXF高剂量组
5%B;29~32 min,5%B),柱温为 30 °C,进样量为 5 μL, 体质量/g a a b b
流速为 0.3 mL/min。(2)质谱条件:采用正、负离子扫描 20 a b
模式进行检测。离子源为电喷雾电离源(ESI),毛细管
18
电压为 3.5 kV,毛细管温度为 350 ℃,鞘气为 45 arb,辅 1 2 3 4 5 6 7
时间/d
助气为 10 arb,源内温度为 350 ℃,质谱采集范围为 m/z A.体质量变化
50~1 500,分辨率为70 000。 39 空白组
2.4.3 样本检测 为保障样本数据采集的重现性与质 38 MXF低剂量组
MXF中剂量组
谱仪器的稳定性,在检测序列中每6个样本添加1个QC MXF高剂量组
样本。将正、负离子模式下采集的所有样本数据连同 肛温/℃ 37
QC 样 本 数 据 进 行 主 成 分 分 析(principal component 36
analysis,PCA),判断仪器的稳定性。 35
2.5 数据处理 1 2 3 4 5 6 7
时间/d
2.5.1 统计学方法 毒性作用指标采用SPSS 20.0软件 B.肛温变化
进行单因素方差分析,数据以x±s表示。检验水准α= a:MXF高剂量组与空白组相比,P<0.05;b:MXF中剂量组与空
白组相比,P<0.05
0.05。采用 GraphPad Prism 9.0 软件进行小鼠生存率
图1 各组小鼠体质量和肛温变化图
分析。
2.5.2 粪便代谢组学数据处理方法 粪便代谢组学原 空白组
100 MXF低剂量组
始数据转换后首先采用R语言软件进行色谱峰识别、对 MXF中剂量组
齐等处理,参数设定使用默认数值,并采用修正 80% 规 MXF高剂量组
则去除缺失值,得到一个保留时间、m/z和峰强度的三维 生存率/% 50
数据矩阵;将得到的数据导入SIMCA-P 17.0软件进行数
据的降维和标准化处理,采用无监督的PCA和有监督的 0
0 2 4 6 8
正交偏最小二乘法-判别分析(orthogonal partial least 时间/d
squares-discriminant analysis,OPLS-DA)对数据进行分 图2 各组小鼠生存率变化图
析,以投影变量重要性(variable importance for the pro‐
3.2 小鼠脏器指数的检测结果
jection,VIP)值>1、方差分析中 P<0.05、倍数变化(fold
与空白组相比,各给药组小鼠的心指数、肝指数、肾
change,FC)>1为条件,筛选得到潜在生物标志物。
指数、精囊腺指数差异均无统计学意义;各给药组小鼠
2.5.3 生物标志物鉴定及代谢通路分析 将“2.5.2”项
的脾指数、肺指数、肾上腺指数均显著升高,胸腺指数显
下获得的潜在生物标志物的保留时间、精确 m/z 以及同
著降低(P<0.05);MXF低、高剂量组小鼠的睾丸指数均
位素比例等信息输入在线数据库 METLIN(https://met‐
显著升高(P<0.05)。结果见表1。
lin.scripps.edu)、HMDB(https://hmdb.ca)进行标志物的
3.3 血清生化指标检测结果
检索和鉴定,使用KEGG数据库(https://kegg.jp)进行代
与空白组相比,各给药组小鼠的心肌功能指标 CK
谢通路分析。
水平显著升高(P<0.05),MXF 低剂量组的 CK-MB/CK
3 结果 比值显著降低(P<0.05);MXF 中剂量组的心肌功能指
3.1 小鼠体质量、肛温和生存率的测定结果 标α-HBDH、LDH 水平均显著升高(P<0.05),肝功能指
灌胃7 d内,空白组小鼠体质量持续增长,肛温维持 标ALP水平显著降低(P<0.05);MXF中、高剂量组的肾
在36~39 ℃范围内,相对稳定。与空白组相比,MXF低 功能指标尿素水平显著升高(P<0.05),CYS-C 水平显
剂量组小鼠体质量增长缓慢,差异无统计学意义;MXF 著降低(P<0.05)。结果见表2~表4。
· 146 · China Pharmacy 2023 Vol. 34 No. 2 中国药房 2023年第34卷第2期