Page 54 - 《中国药房》2022年22期
P. 54
表2 正交实验设计方案与结果 5 诃黎勒酸 5 诃黎勒酸
诃子酸
诃子酸
实验编号 A B C D 诃黎勒酸含量/(mg/g) 诃子酸含量/(mg/g) 综合评分 4 4
1 1 1 1 1 43.19 19.23 29.03 ( mg/mL ) 3 ( mg/mL ) 3
2 1 2 2 2 114.26 50.09 76.30 2 2
3 1 3 3 3 110.39 42.40 69.88 浓度/ 1 浓度/ 1
4 2 1 2 3 71.62 38.47 52.35
0 0
5 2 2 3 1 90.28 48.46 65.96
0 2 4 6 8 10 0 2 4 6 8 10
6 2 3 1 2 110.60 57.32 79.50
柱体积 柱体积
7 3 1 3 2 115.57 69.58 89.27 A. 1.0 g/mL上样液 B. 0.5 g/mL上样液
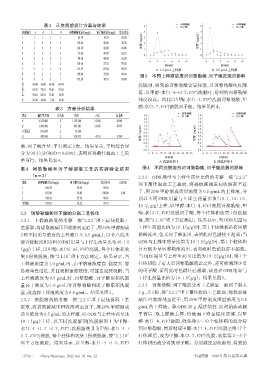
8 3 2 1 3 129.06 72.94 96.64 图3 不同上样液浓度对诃黎勒酸、诃子酸洗脱的影响
9 3 3 2 1 127.50 78.19 99.40
58.40 56.88 68.38 64.79
K 1 洗脱时,得到的诃黎勒酸含量较低,且诃黎勒酸纯度降
65.93 79.63 76.01 81.69
K 2 低;以甲醇-水(1∶4→3∶7,V/V)洗脱时,得到的诃黎勒酸
95.10 82.91 75.03 72.95
K 3
R 36.70 26.04 7.63 16.90 纯度较高。因此以甲醇-水(1∶4,V/V)洗脱诃黎勒酸,甲
表3 方差分析结果 醇-水(3∶7,V/V)洗脱诃子酸。结果见图4。
诃黎勒酸 诃黎勒酸
因素 偏差平方和 自由度 均方 F比 显著性 1.8 诃子酸 1.8 诃子酸
1.6 1.6
A 2 254.480 2 1 127.240 21.836 0.044 1.4 1.4
B 1 206.402 2 603.201 11.685 0.079 1.2 1.2
C(误差) 103.247 2 51.624 ( mg/mL ) 1.0 ( mg/mL ) 1.0
0.8
0.8
D 428.746 2 214.373 4.153 0.194 0.6 0.6
浓度/ 0.4 浓度/ 0.4
0.2 0.2
酸、诃子酸含量,平行测定3次。结果显示,平均综合评 0 0
-0.2 -0.2
分为99.33分(RSD=0.68%),表明所得最佳提取工艺简 -5 0 5 10 15 20 25 30 35 40 45 -5 0 5 10 15 20 25 30 35 40 45
柱体积 柱体积
单可行。结果见表4。 A.洗脱溶剂Ⅰ B.洗脱溶剂Ⅱ
表4 诃黎勒酸和诃子酸提取工艺的实验验证结果 图4 不同洗脱溶剂对诃黎勒酸、诃子酸洗脱的影响
(n=3) 2.3.3 ODS 用量与上样生药量比值的考察 按“2.2.3”
批次 诃黎勒酸含量/(mg/g) 诃子酸含量/(mg/g) 综合评分 RSD/% 项下最佳提取工艺提取,将提取液减压回收溶剂至近
1 106.74 58.59 99.34
2 107.48 58.82 100.00 0.68 干,用 20% 甲醇制成质量浓度为 0.5 g/mL 的上样液,分
3 106.92 57.56 98.65 别以不同 ODS 用量与上样生药量比值(10∶1、10∶1.5、
平均值 107.05 58.32 99.33
10∶2,g/g)上样,以甲醇-水(1∶4,V/V)洗脱诃黎勒酸,甲
2.3 诃黎勒酸和诃子酸的分离工艺优化 醇-水(3∶7,V/V)洗脱诃子酸,每个柱体积收集 1 份洗脱
2.3.1 上样液浓度的考察 按“2.2.3”项下最佳提取工 液,按“2.1.10”项下方法测定。结果显示,当ODS用量与
艺提取,将提取液减压回收溶剂至近干,用35%甲醇制成 上样生药量比值为10∶1(g/g)时,第1个柱体积虽有诃黎
2种不同质量浓度的上样液(1.0、0.5 g/mL),以十八烷基 勒酸流出,但无诃子酸流出,表明此时色谱柱不超载;当
键合硅胶反相填料(ODS)用量与上样生药量比为10∶1.5 ODS与上样生药量比值为10∶1.5(g/g)时,第1个柱体积
(g/g)上样,以甲醇-水(35∶65,V/V)洗脱,每个柱体积收 只有极少量诃黎勒酸流出,表明此时色谱柱亦不超载;
集 1 份洗脱液,按“2.1.10”项下方法测定。结果显示,当 当 ODS 用量与上样生药量比值为 10∶2(g/g)时,第 1 个
上样液浓度为1.0 g/mL时,由于溶液浓度高、黏度大,容 柱体积除了有大量诃黎勒酸流出之外,还可检测到少量
易堵塞色谱柱,并且吸附速度较慢,可能造成死吸附;当 的诃子酸,证明此时色谱柱已超载,故选择 ODS 用量与
上样液浓度为 0.5 g/mL 时,诃黎勒酸、诃子酸累积洗脱 上样生药量比值为10∶1.5(g/g)。结果见图5。
量高于浓度为 1.0 g/mL 时诃黎勒酸和诃子酸累积洗脱 2.3.4 诃黎勒酸、诃子酸的分离工艺验证 取诃子粉末
量,故选择上样液浓度为0.5 g/mL。结果见图3。 3 g,共3份,按“2.2.3”项下最佳提取工艺提取,将提取液
2.3.2 洗脱溶剂的考察 按“2.2.3”项下最佳提取工艺 减压回收溶剂至近干,用 20% 甲醇制成质量浓度为 0.5
提取,将提取液减压回收溶剂至近干,用 20% 甲醇制成 g/mL的上样液。取ODS 20 g,湿法装柱,以初始流动相
质量浓度为0.5 g/mL的上样液,以ODS与上样生药量比 平衡后,取上样液上样,待液面下降至柱床顶部,以甲
10∶1(g/g)上样,以不同洗脱溶剂[洗脱溶剂Ⅰ为甲醇- 醇-水(1∶4,V/V)洗脱,收集第 2~10 个柱体积的流分得
水(1∶4→1∶3→3∶7,V/V),洗脱溶剂Ⅱ为甲醇-水(1∶4→ 到诃黎勒酸,然后继续甲醇-水(1∶4,V/V)洗脱至第17个
3∶7,V/V)]洗脱,每个柱体积收集1份洗脱液,按“2.1.10” 柱体积后,改为甲醇-水(3∶7,V/V)洗脱,收集第 2~5 个
项下方法测定。结果显示,以甲醇-水(1∶4→1∶3,V/V) 柱体积的流分得到诃子酸。分别减压回收溶剂,得到的
· 2736 · China Pharmacy 2022 Vol. 33 No. 22 中国药房 2022年第33卷第22期