Page 125 - 《中国药房》2022年11期
P. 125
多靶点 10 1 1 2 n=1
EGFR 7 1 1 1 n=3
HER2 2 2 3 1 n=3
PD-1 1 4 3 n=4
VEGFR 3 1 2 n=4
PAPR 1 1 2 n=3
ALK 1 1 1 n=1
BTK 1 1 n=1
CDK 1 1
BCL-2 1
CD19 1
CD20 1
CD30 1
CD38 1 2018年版《指导原则》中作用于相应靶点的药物品种数量
CTAL-4 1 2019年版《指导原则》中新增作用于相应靶点的药物品种数量
FLT3 1 2020年版《指导原则》中新增作用于相应靶点的药物品种数量
HDAC 1 n=1
JAK 1 2021年版《指导原则》中新增作用于相应靶点的药物品种数量
MEK 1
MET 1
mTOR 1
PSMB 1
RANKL 1
RET 1
0 2 4 6 8 10 12 14 16
品种数量
n:作用于相应靶点的国产原研品种数量
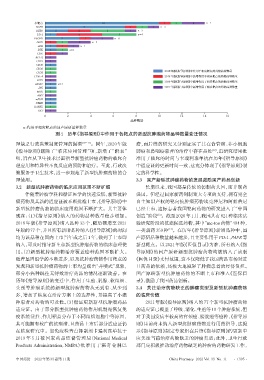
图4 历年《指导原则》中作用于各靶点的新型抗肿瘤药物品种数量变迁情况
理缺乏行政决策制度管理的漏洞 [10-11] 。同年,2020年版 瘤,而后续的研究又分别证实了其在食管癌、非小细胞
[12]
《指导原则》删除了“临床应用管理”项,新增了“附表” 肺癌和鼻咽癌患者的治疗中存在益处 ,且研究结果批
项,旨在从卫生技术层面指导新型抗肿瘤药物的临床合 准用于临床的时间与卡瑞利珠单抗在历年《指导原则》
理应用和特异性不良反应的预防和治疗。至此,行政决 中适应证的更新时间一致,这充分体现了《指导原则》制
策服务于卫生技术,进一步规范了新型抗肿瘤药物的合 定的科学性。
理使用。 3.3 国产新型抗肿瘤药物的发展激励国产药品创新
3.2 新型抗肿瘤药物的临床应用范围不断扩增 长期以来,我国都是传统的仿制药大国,而非制药
伴随着肿瘤学科和循证医学的快速发展,新型抗肿 强国。但经过国家新药创制重大专项的支持,拥有完全
瘤药物及其新的适应证被不断批准上市,《指导原则》中 自主知识产权的靶向抗肿瘤药物埃克替尼和阿帕替尼
新型抗肿瘤药物的临床应用范围不断扩大。其主要体 已经上市,这标志着我国靶向药物的研发进入了“中国
[13]
现在:(1)《指导原则》纳入的药物品种数量稳步增加。 创造”阶段 。截至2020年1月,我国共有821种临床试
2018 年版《指导原则》纳入品种 33 个,随后骤增至 2021 验研究阶段的抗癌候选药物,其中“me-too药物”404种,
年版的77个,并且所有新增品种纳入《指导原则》的时间 一类新药 359 种 。在历年《指导原则》新增品种中,国
[14]
均为该品种在国内上市当年或之后1年,做到了上市即 产原研品种数量越来越多,且主要作用于PD-1、PAPR等
纳入,可及时指导新上市新型抗肿瘤药物的临床合理使 新型靶点。以2021年版《医保目录》为准,所有纳入《指
用。(2)新型抗肿瘤药物治疗覆盖癌种范围不断扩大。 导原则》的国产原研新型抗肿瘤药物均被纳入了该版
随着基因组学的不断进步,以及抗肿瘤药物作用靶点的 《医保目录》支付范围,这不仅降低了我国药品市场对进
发现和新型抗肿瘤药物的上市均呈现出“井喷式”现象, 口药品的依赖,还极大地减轻了肿瘤患者的经济负担。
部分小癌种既往无特效治疗药品的情况逐渐改善。在 国产原研新型抗肿瘤药物的不断上市和准入《医保目
历年《指导原则》的变迁中,作用于生殖、乳腺、软组织、 录》,激励了我国药品创新。
头颈等肿瘤系统的新型抗肿瘤药物从无到有、从少到 3.4 关注治疗药物缺乏的肿瘤类型及新型抗肿瘤药物
多,增加了临床在治疗方案上的选择性,并提高了小癌 的临床价值
种患者对药物的可及性。(3)循证更新新型抗肿瘤药品 2021年版《指导原则》纳入的77个新型抗肿瘤药物
适应证。由于部分新型抗肿瘤药物作用机制是恢复免 的适应证已覆盖了呼吸、消化、生殖等10个肿瘤系统,但
疫系统活性、作用靶点分布于不同组织细胞中等原因, 对于我国发病率较高的宫颈癌、膀胱癌等癌种,《指导原
其可能拥有较广的抗瘤谱,且药品上市后部分适应证仍 则》目前尚未纳入新型抗肿瘤药物进行用药指导,这提
在临床研究中。如免疫检查点抑制剂卡瑞利珠单抗于 示《指导原则》制定专家组在后续《指导原则》的更新中
2019 年 5 月被国家药品监督管理局(National Medical 应关注当前治疗药物缺乏的肿瘤类型;此外,卫生行政
Products Administration,NMPA)批准用于霍奇金淋巴 部门应积极推动治疗药物缺乏的肿瘤的药物研发工作,
中国药房 2022年第33卷第11期 China Pharmacy 2022 Vol. 33 No. 11 ·1395 ·