Page 63 - 《中国药房》2021年21期
P. 63
量/水溶性浸出物含量最大值×0.372 3+芍药内酯苷含量/ 详见图2。由图2可知,A与B的交互作用较强。以该软
芍药内酯苷含量最大值×0.233 9+氧化芍药苷含量/氧化 件求解上述二元回归方程,得到酒赤芍的最优炮制工艺
芍药苷含量最大值×0.131 7+苯甲酸含量/苯甲酸含量最 为闷润时间35 min、炒制时间20 min、炒制温度120 min;
大值×0.078 9)×100。 模型预测值为98.75。
表 6 3 种权重分析方法所得的酒赤芍炮制工艺综合 1.00 综合评分
8
评分 7 6 0.50
Tab 6 Comprehensive evaluation of three weighting 综合评分 5 4 min 0
methods of P. lactiflora stir-baked with wine 3 2 B,
-0.50
序号 AHP法 CRITIC法 AHP-CRITIC混合加权法 1.00 1.00
0.50 0.50
1 86.58 80.73 72.64 0 0 -1.00
B,min -0.50 -0.50 A,min -1.00 -0.50 0 0.05 1.00
2 88.76 81.57 80.03 -1.00 -1.00 A,min
3 92.41 83.16 84.37 a. A-B交互作用(响应面图) b. A-B交互作用(等高线图)
4 77.88 69.95 69.98 1.00 综合评分
5 85.67 58.95 54.68 8
7
6 74.52 66.22 66.65 6 0.50
7 59.66 76.09 75.35 综合评分 5 4 ℃ 0
8 83.11 71.62 73.11 3 2 C,
9 91.64 83.28 82.21 -0.50
1.00 1.00
10 74.74 67.90 67.34 0.50 0 0 0.50 -1.00
11 87.80 78.18 76.24 C,℃ -0.50 -0.50 A,min -1.00 -0.50 0 0.05 1.00
-1.00 -1.00
12 59.74 58.48 59.50 A,min
c. A-C交互作用(响应面图) d. A-C交互作用(等高线图)
13 60.34 57.57 54.88
综合评分
14 80.86 69.97 73.63 1.00
8
15 59.66 76.09 75.35 7 0.50
16 76.89 69.25 68.81 综合评分 6 5
17 91.83 81.08 82.22 4 3 ℃ C, 0
2
2.7 模型拟合及验证实验 -0.50
1.00 1.00
2.7.1 模型拟合 以综合评分为因变量,以因素A、B、C 0.50 0 0 0.50 -1.00
C,℃ -0.50 -0.50 B,min -1.00 -0.50 0 0.05 1.00
为自变量,应用Design-Expert 8.0.6.1软件进行二次多元 -1.00 -1.00
B,min
回归拟合模型分析,得到回归方程为:综合评分=4.45+ e. B-C交互作用(响应面图) f. B-C交互作用(等高线图)
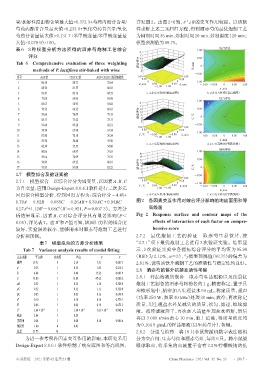
0.70A - 0.82B - 0.085C - 0.26AB + 0.39AC + 0.94BC - 图2 各因素交互作用对综合评分影响的响应面图和等
0.27A +1.12B -0.68C(R =0.921,P=0.007 3)。方差分 高线图
2
2
2
2
析结果显示,因素 B、C 对综合评分具有显著影响(P< Fig 2 Response surface and contour maps of the
0.05),详见表7。由R 和P值可知,该回归方程的拟合度 effects of interaction of each factor on compre-
2
较好,实验误差较小,能够用来对酒赤芍炮制工艺进行 hensive score
分析和预测。 2.7.2 最优炮制工艺的验证 取赤芍生品饮片,按
表7 模型拟合的方差分析结果 “2.7.1”项下最优炮制工艺进行 3 次验证实验。结果显
Tab 7 Variance analysis results of model fitting 示,3 次验证实验中各指标综合评分的平均值为 95.98
方差来源 平方和 自由度 均方 F P (RSD 为 2.12%,n=3),与模型预测值(98.75)的偏差为
模型 19.71 9 2.19 7.51 0.007 3 2.81%,说明该饮片酒制工艺的准确性与稳定性均良好。
A 0.53 1 0.53 1.83 0.218 5 2.8 酒赤芍的体外抗凝血活性考察
B 4.44 1 4.44 15.22 0.005 9
C 13.89 1 13.89 47.62 0.000 2 2.8.1 样品溶液的制备 取赤芍生品粗粉以及按最优
AB 0.32 1 0.32 1.10 0.328 4 炮制工艺制备的酒赤芍粗粉各约1 g,精密称定,置于具
AC 0.32 1 0.32 1.11 0.328 0 塞锥形瓶中,精密加入生理盐水50 mL,称定质量,超声
BC 0.05 1 0.05 0.16 0.698 4
A 2 0.10 1 0.10 0.34 0.579 1 (功率 250 W,频率 40 kHz)处理 30 min,放冷;再次称定
B 2 0.06 1 0.06 0.19 0.672 3 质量,用生理盐水补足减失的质量,摇匀,滤过,取续滤
C 2 1.64×10 -3 1 1.64×10 -3 5.61×10 -3 0.942 4 液。将续滤液蒸干,再次加入适量生理盐水溶解,然后
残差 2.04 7 0.29 再以 3 000 r/min 离心 10 min,取上清液,得质量浓度均
失拟项 0.24 3 0.08 0.18 0.906 6
纯误差 1.80 4 0.45 为0.104 9 g/mL的样品溶液(以生药量计),备用。
总差 21.75 16 2.8.2 分组与给药 将 18 只小鼠按随机数字表法随机
为进一步考察各因素交互作用的影响,本研究采用 分为空白组、生赤芍组和酒赤芍组,每组6只。将小鼠摘
Design-Expert 8.0.6.1软件绘制了响应面图和等高线图, 眼球取血,将采集的血液置于含有 3.2%柠檬酸钠的抗
中国药房 2021年第32卷第21期 China Pharmacy 2021 Vol. 32 No. 21 ·2617 ·