Page 24 - 《中国药房》2021年21期
P. 24
5 提示函制度实施情况分析 就提示函中的风险信息积极开展排查、分析和验证并将
本文对2014-2020年提示函的整体情况进行分析, 排查整改情况反馈给国家药监局。2020 年,312 份提示
并对最新的2020年提示函总体情况、排查情况和整改情 函中有6份中药饮片的提示函由于涉及的6家生产企业
况、排查后仍存在的问题等进行分析,结果如下。 已注销,不会继续生产药品或继续产生风险,故无排查
5.1 2014-2020年提示函整体情况 必要。因此,在产的 280 家生产企业对 306 份提示函中
2014-2020 年,国家药监局已向 2 323 家次的生产 的问题开展了排查,排查情况如表2所示。其中,以生产
企业发出 2 837 份提示函,涉及化学药、中成药、中药饮 企业根据提示函对药品生产全过程各环节开展排查并
片、生物制品、包材、辅料等各个类别的产品。由于每年 找到被提示的问题视为准确提示。从排查结果来看,各
国家药品抽检的具体药品不同,其质量状况各不相同, 类药品排查发现问题的提示准确率均超过85%,整体准
因此每年的提示函数量及被提示生产企业数量也随之 确率达 87.91%,说明 2020 年提示函具有较为满意的科
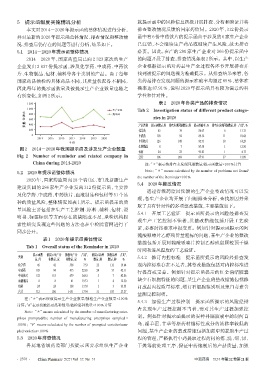
有所变化,如图2所示。 学性和针对性。
1 200 表2 2020年各类产品的排查情况
1 000 生产企业 Tab 2 Investigation status of different product catego-
件/家次 800 提示函 ries in 2020
600
数量, 400 产品类别 提示函数量,件 排查发现问题数量,件 提示准确率,% 排查未发现问题数量,件 占比 ,%
*
200 化学药 45 39 86.67 6 13.33
0 中成药 103 92 89.32 11 10.68
2014 2015 2016 2017 2018 2019 2020
年份 中药饮片 126 108 85.71 18 14.29
生物制品 8 7 87.50 1 12.50
图2 2014-2020年我国提示函及涉及生产企业数量
包材 24 23 95.83 1 4.17
Fig 2 Number of reminder and related company in 合计 306 269 87.91 37 12.09
China during 2014-2020 注:“*”表示按排查未发现问题数量/提示函数量×100%计算
5.2 2020年提示函整体情况 Note:“*”means calculated by the number of problems not found/
the number of the Reminder×100%
2020年,国家药监局向28个省(区、市)及新疆生产
5.4 2020年整改情况
建设兵团的 286 家生产企业发出 312 份提示函,主要涉
通过省级药监局反馈的生产企业整改情况可以发
及化学药、中成药、中药饮片、血液制品和包材等51个品
现,各生产企业均开展了问题排查分析,查找原因并采
种的质量风险,整体情况如表1所示。提示函提示的质
取了具有针对性的多项整改措施,主要措施如下。
量风险主要包括在生产工艺控制、原料、辅料、包材、说
5.4.1 开展工艺验证 提示函所提示的风险经排查发
明书、标签标识等方面存在的缺陷或不足,承检机构探
现生产工艺控制不佳者,其整改措施包括开展工艺验
索性研究发现这些问题的方法也在中检院官网进行了
证,必要时按要求申报变更。例如针对提示函提示的阿
同步公开。
魏酸哌嗪片乙醇残留量超标的问题,某生产企业的整改
表1 2020年提示函整体情况
措施包括开展阿魏酸哌嗪片控制乙醇残留颗粒预干燥
Tab 1 Overall status of the Reminder in 2020
时间和进风温度的工艺验证。
*
#
提示函数 被提示生产企 抽检生产企 占比 , 被提示品种 抽检品种 占比 ,
类别 5.4.2 修订内控标准 提示函所提示的风险经排查发
量,件 业数量,家 业数量,家 % 数量,种 数量,种 %
化学药 45 42 558 7.53 22 112 19.64 现内控标准存在不足者,其整改措施包括对内控标准进
中成药 103 94 415 22.65 24 57 42.11 行提高或完善。例如针对提示函提示的红金消结胶囊
中药饮片 132 118 479 24.63 3 7 42.86
血液制品 8 8 41 19.51 1 8 12.50 缺少石细胞特征的问题,某生产企业的整改措施包括修
包材 24 24 138 17.39 1 3 33.33 订成品内控质量标准,增订石细胞鉴别项及鬼臼毒素含
合计 312 286 1 631 17.54 51 187 27.27
量测定控制项。
注:“*”表示按被提示生产企业数量/抽检生产企业数量×100%
5.4.3 加强生产过程控制 提示函所提示的风险经排
计算;“#”表示按被提示品种数量/抽检品种数量×100%计算
查发现生产过程控制不当者,需对其生产过程加强控
Note:“*”means calculated by the number of manufacturing enter-
制。例如针对提示函提示的安神补脑胶囊中的制何首
prises prompted/the number of manufacturing enterprises sampled ×
100%;“#”means calculated by the number of prompted varieties/sam- 乌、淫羊藿、甘草等原药材指标性成分的转移率较低的
pled varieties×100% 问题,某生产企业的整改措施包括加强中药提取生产过
5.3 2020年排查情况 程的管理,严格执行中药提取过程药材的拣、洗、润、切、
各属地省级药监部门按提示函要求组织生产企业 干燥等前处理工序,保证中药炮制后的产品质量,加强
·2578 · China Pharmacy 2021 Vol. 32 No. 21 中国药房 2021年第32卷第21期