Page 77 - 《中国药房》2021年2期
P. 77
表3 肝微粒体孵育体系中5种代谢产物的回归方程与 组平行3次。按“2.6”项下方法制备孵育体系,试验组孵
线性范围 育体系中分别加入质量浓度为 50.0、15.0、5.0、1.5、0.5、
Tab 3 Regression equation and linear range of 5 me- 0.15、0.05 μmol/L 的树豆酮酸 A 溶液,阳性对照组孵育
tabolites in liver microsome incubation system 体 系 中 分 别 加 入“2.4”项 下 的 α- 萘 黄 酮 、奎 尼 丁 、
(+)-N-3-苄基香酚、酮康唑、磺胺苯吡唑溶液,空白组孵
待测物 线性方程 R 2 线性范围,μmol/L
对乙酰氨基酚 y=0.041 0x+0.183 3 0.999 3 0.26~8.35 育体系中加入等体积的 PBS。按“2.7.1”项下方法处理
右啡烷 y=0.019 1x-0.031 1 0.996 4 0.36~34.56 后,按“2.7”项下方法分析各探针药物对应的代谢产物对
5-羟基奥美拉唑 y=0.035 0x-0.577 6 0.993 6 0.10~3.09 乙酰氨基酚、右啡烷、5-羟基奥美拉唑、6β-羟基睾酮和羟
6β-羟基睾酮 y=0.038 1x+0.087 8 0.999 4 3.67~117.37
羟基甲苯磺丁脲 y=0.041 4x+0.081 7 0.993 5 0.15~4.88 基甲苯磺丁脲的含量。以空白组代谢产物的含量记为
c0,其余各组的代谢产物含量记为 cx,计算剩余酶活性,
后进样测定,考察稳定性。另取空白肝微粒孵育体系
剩余酶活性(%)=(1-cx/c0 )×100%。以树豆酮酸 A 的
200 μL,置于2 mL EP管内,按“2.7.1”项下方法处理样品
质量浓度(x,μmol/L)为横坐标、剩余酶活性(y,%)为纵
后,用氮气流吹干,分别加入对乙酰氨基酚、右啡烷、5-
坐标,使用Graphpad Prism 5.0软件进行非线性回归分析
羟基奥美拉唑、6β-羟基睾酮、羟基甲苯磺丁脲标准溶液
并计算半数抑制浓度(IC50 )。肝微粒体中 CYP1A2、
适量,使其质量浓度与上述样品对应,每个浓度平行 5
CYP2D6、CYP2C19、CYP3A4、CYP2C9 酶的剩余酶活
份,进样测定,记录峰面积(A1 );以甲醇配制相应浓度且
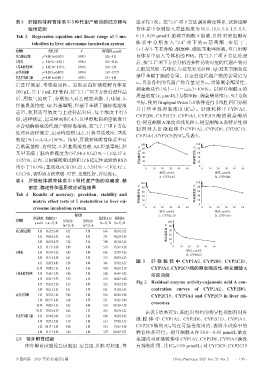
性-树豆酮酸A浓度曲线见图3,树豆酮酸A和特异性抑
不含辅酶溶液的代谢产物标准溶液,按“2.7.1”项下方法
制 剂 对 人 肝 微 粒 体 中 CYP1A2、CYP2D6、CYP2C19、
处理后进样测定,记录峰面积(A2 ),计算基质效应,基质
CYP3A4、CYP2C9的IC50见表5。
效应(%)=A1/A2×100%。结果,肝微粒体孵育体系中对
乙酰氨基酚、右啡烷、5-羟基奥美拉唑、6β-羟基睾酮、羟 % 100 % 100
80
80
基甲苯磺丁脲的准确度为(87.04±8.62)%~(102.37± 剩余酶活性, 60 剩余酶活性, 60
4.85)%,日内、日间精密度试验和12 h稳定性试验的RSD 40 40
20
20
均小于10.0%;基质效应为(84.22±3.58)%~(102.42± 0 0 10 20 30 40 50 0 0 10 20 30 40 50
6.51)%,表明该方法准确、可靠、重现性好,详见表4。 浓度,μmol/L 浓度,μmol/L
A. CYP1A2 B. CYP2D6
表 4 肝微粒体孵育体系中 5 种代谢产物的准确度、精
100 100
密度、稳定性和基质效应试验结果 % 80 % 80
Tab 4 Results of accuracy,precision,stability and 剩余酶活性, 60 剩余酶活性, 60
40
40
matrix effect tests of 5 metabolites in liver mi- 20 20
0 0
crosome incubation system 0 10 20 30 40 50 0 10 20 30 40 50
浓度,μmol/L 浓度,μmol/L
精密度 C. CYP2C19 D. CYP3A4
质量浓度,准确度(x± 稳定性RSD 基质效应
待测物 日内RSD 日间RSD 100
μmol/L s,n=5),% (n=5),% (n=5),%
(n=5),% (n=3),% % 80
对乙酰氨基酚 0.26 96.22±6.98 8.22 9.38 6.46 90.24±6.22 剩余酶活性, 60
0.52 94.86±3.23 6.61 8.32 7.31 84.22±3.58 40
20
2.09 88.87±4.79 7.28 9.56 3.98 88.74±5.22
0
8.35 91.13±8.28 9.89 8.84 5.93 93.56±4.28 0 10 20 30 40 50
右啡烷 0.36 98.34±8.22 8.02 9.04 8.46 92.70±8.26 浓度,μmol/L
E. CYP2C9
0.36 91.11±4.28 6.61 7.24 7.12 89.82±6.53
8.71 92.82±4.85 7.28 8.08 3.46 92.42±6.27 图 3 肝 微 粒 体 中 CYP1A2、CYP2D6、CYP2C19、
21.78 90.88±1.23 4.31 5.64 4.30 94.22±2.18 CYP3A4、CYP2C9酶的剩余酶活性-树豆酮酸A
5-羟基奥美拉唑 0.10 95.86±8.92 9.46 9.88 6.88 96.44±8.92 浓度曲线
0.19 92.61±9.79 5.39 6.36 2.93 86.82±6.20
0.77 95.63±2.28 3.25 4.43 3.22 99.36±3.28 Fig 2 Residual enzyme activity-cajanonic acid A con-
3.09 98.11±3.25 4.31 5.38 8.21 91.82±5.53 centration curves of CYP1A2, CYP2D6,
6β-羟基睾酮 3.67 92.74±3.42 9.62 9.82 8.36 88.04±9.28 CYP2C19,CYP3A4 and CYP2C9 in liver mi-
7.34 102.37±4.85 6.28 6.78 7.21 92.42±8.04 crosomes
29.34 94.86±3.23 8.26 8.44 5.18 102.38±3.58
117.37 92.87±4.79 6.66 7.25 4.55 98.72±5.22 由表 5 结果可知,阳性对照组的特异性抑制剂对肝
羟基甲苯磺丁脲 0.15 87.04±8.62 7.16 7.82 8.68 98.28±8.32 微 粒 体 中 CYP1A2、CYP2D6、CYP2C19、CYP3A4、
0.30 98.25±8.24 3.18 3.02 6.13 97.50±3.12
1.22 101.71±8.24 4.68 5.82 9.23 93.56±4.28 CYP2C9 酶的 IC50均在可接受范围内,表明本试验中的
4.88 91.11±4.28 5.84 6.88 5.07 102.42±6.51 孵育体系可行。树豆酮酸 A 在 50.0~0.05 μmol/L 浓度
2.8 体外孵育试验 范围内对肝微粒体中 CYP1A2、CYP2D6、CYP3A4 酶没
体外孵育试验设置试验组、空白组、阳性对照组,每 有抑制作用,其 IC50>50 μmol/L;对 CYP2C9、CYP2C19
中国药房 2021年第32卷第2期 China Pharmacy 2021 Vol. 32 No. 2 ·199 ·