Page 16 - 《中国药房》2020年22期
P. 16
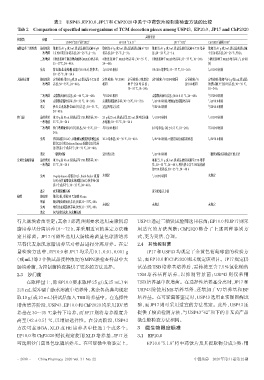
表2 USP43、EP10.0、JP17和ChP2020中关于中药饮片控制菌检查方法的比较
Tab 2 Comparison of specified microorganisms of TCM decoction pieces among USP43,EP10.0,JP17 and ChP2020
具体要求
控制菌 步骤
USP43“2021”和“2022” EP10.0“2.6.31” JP17“5.02” ChP2020“通则1108”
耐胆盐革兰阴性菌 前处理及 取相当于l g 或l mL供试品的供试液至pH 取相当于l g 或l mL供试品的供试液至TSB 取相当于l g 或l mL供试品的供试液至TSB培养 取相当于l g 或l mL供试品的供试液
一次增菌 7.2 PBS或TSB培养基;20~25 ℃,2~5 h 培养基;20~25 ℃,2~3 h 基;20~25 ℃,2~5 h 至TSB培养基;20~25 ℃,约2 h
二次增菌 3浓度接种于肠道增菌液体(MEEB)培养基; 4 浓度接种于 MEEB 培养基;30~35 ℃, 3浓度接种于MEEB培养基;35~37 ℃,18~24 h 3浓度接种于MEEB培养基;与EP相
35~37℃,24~48 h 24~48 h 同
分离 紫红胆盐葡萄糖琼脂(VRGBA)培养基; 与USP43相同 VRGBA培养基;35~37 ℃,18~24 h 与USP43相同
30~35 ℃,18~24 h
大肠埃希菌 前处理及 定性检验:取10 g或10 mL供试品至TSB培 定性检验:与USP43 定量检验:3浓度接 定性检验:与USP43相同 定量检验:与 定性检验:取相当于l g 或l mL供试品
一次增菌 养基;30~35℃,24~48 h 相同 种于 TSB 培养基; EP10.0相同 的供试液至TSB培养基;30~35 ℃,
30~35℃,18~24 h 18~24 h
二次增菌 麦康凯肉汤培养基;42~44 ℃,24~48 h 与USP43相同 麦康凯肉汤培养基;(44±0.5)℃,24~48 h 与USP43相同
分离 麦康凯琼脂培养基;30~35 ℃,18~24 h 麦康凯琼脂培养基;30~35℃,18~72 h 与EP10.0相同;增加显色琼脂培养基 与EP10.0相同
鉴定 伊红美蓝琼脂(EMB)培养基;30~35 ℃, 适宜的鉴定方法 与EP10.0相同 与EP10.0相同
24~48 h
沙门菌 前处理及 取10 g或10 mL供试品至TSB培养基;30~ 25 g或25 mL供试品至225 mL缓冲蛋白胨 与USP43相同 与USP43相同
一次增菌 35 ℃,18~24 h 水溶液;30~35 ℃,18~24 h
二次增菌 沙门增菌液体(RV)培养基;30~35℃,18~ 与USP43相同 RV培养基;(42±0.5)℃,18~24 h 与USP43相同
24 h
分离 亮绿琼脂(BGA)、木糖赖氨酸脱氧胆酸盐琼 XLD培养基;30~35 ℃,18~48 h 与EP10.0相同;可选用显色琼脂培养基 与EP10.0相同
脂(XLD)或Hektoen Enteric琼脂(HE)培养
基(任选1个或多个);30~35 ℃,24~48 h
鉴定 三糖铁试验 适宜的方法 与EP10.0相同 三糖铁试验或其他适宜的方法
金黄色葡萄球菌 前处理及 取10 g或10 mL供试品至TSB培养基;30~ 取相当于l g 或l mL供试品的供试液至TSB培养
一次增菌 35 ℃,18~24 h 基,30~35 ℃,24~48 h,再转接至含7.5%氯化钠
的TSB培养基,30~35 ℃,24~48 h
分离 Vogel-Johnson 琼脂(VJ)、Baird-Parker 琼脂 未规定 与USP43相同 未规定
(BP)或甘露醇氯化钠琼脂(MS)培养基(任
选1个或多个);30~35 ℃,24~48 h
鉴定 血浆凝固酶试验 适宜的鉴定方法
梭菌 前处理 取样2份,单份80 ℃加热10 min
增菌 梭菌增菌肉汤培养基;厌氧35~37℃,48 h
未规定 未规定 未规定
分离 哥伦比亚琼脂培养基;厌氧35~37℃,48 h
鉴定 氧气利用试验、氧化酶试验
行大肠埃希菌鉴定;其余3部药典则要求选用麦康凯琼 USP43通过三糖铁试验筛选目标菌;EP10.0和JP17则采
脂培养基分离培养18~72 h,并采用适宜的鉴定方法确 用适宜的方法判断;ChP2020 整合了上述两种鉴别方
定目标菌。JP17 可额外选用大肠埃希菌显色琼脂培养 式,更为灵活、合理。
基替代麦康凯琼脂培养基对样品进行分离培养。在定 2.4 其他控制菌
量检验方法中,EP10.0 和 JP17 均采用 0.1、0.01、0.001 g JP17 和 USP43 均规定了金黄色葡萄球菌的检验方
(或mL)等3个供试品接种浓度的MPN法检查样品中大 法,而EP10.0和ChP2020则未规定该项目。JP17规定供
肠埃希菌,为控制菌检查提供了更多的方法选择。 试品经 TSB 培养基培养后,需转接至含 7.5%氯化钠的
2.3 沙门菌 TSB 培养基再培养,以抑制背景菌;USP43 则仅采用
在取样量上,除 EP10.0 要求取样 25 g(或 25 mL)至 TSB培养基单次增菌。在选择性培养基分离时,JP17和
225 mL缓冲蛋白胨水溶液中培养外,其余各药典均规定 USP43 除使用 MS 培养基外,还增加了 VJ 培养基和 BP
取10 g(或10 mL)供试品加入TSB培养基中。在选择性 培养基。在可疑菌落鉴定时,USP43选用血浆凝固酶试
增菌培养阶段,USP43、EP10.0 和 ChP2020 均采用 RV 培 验,而 JP17 则可采用适宜的方法鉴定。此外,USP43 还
养基在 30~35 ℃条件下培养,而 JP17 则将培养温度升 提供了梭菌检测方法,与USP43“62”项下的非无菌产品
高至(42±0.5)℃,以增加选择性。在分离阶段,USP43 微生物检查方法相同。
方法可在 BGA、XLD 或 HE 培养基中任选 1 个或多个; 3 微生物限度标准
EP10.0 和 ChP2020 则仅规定使用 XLD 培养基,JP17 还 3.1 EP10.0
可选用沙门菌显色琼脂培养基。在可疑微生物鉴定上, EP10.0“5.1.8”将中药饮片及其提取物分成 3 类:用
·2698 · China Pharmacy 2020 Vol. 31 No. 22 中国药房 2020年第31卷第22期