Page 89 - 202010
P. 89
0.10 0.20 2
0.18
0.08
0.16
0.06 0.14
AU 0.12
0.04 0.10 8
0.02 AU 0.08
0 0.06
0.04 10
0 10 20 30 40 50 60 70 0.02 1 3 6 11
t,min 0
A.阴性溶液 -0.02
0 10 20 30 40 50 60 70 80
0.10 2 t,min
A.未破坏溶液
0.08
0.020 2
0.06
AU 0.015
0.04
3 0.010
0.02 5 AU
1 4 7 9
0 0.005
0 10 20 30 40 50 60 70 1 3 4 7
t,min 0
B.对照品混合溶液
0 10 20 30 40 50 60 70 80
0.20 t,min
0.18 2
0.16 B.酸破坏溶液
0.14 0.020 2
0.12 8
AU 0.10
0.08 0.015
0.06
0.04 10 AU 0.010
0.02 1 3 6 11
0
0.005
0 10 20 30 40 50 60 70 1 3 4
t,min 0
C.供试品溶液
0 10 20 30 40 50 60 70 80
0.014 2 8 10 t,min
0.012
0.010 11 C.碱破坏溶液
0.008 3 0.020 2
AU 0.006
0.004 7 9 0.015
0.002 1 4 5 6
0 AU 0.010
-0.002
0 10 20 30 40 50 60 70
0.005
t,min
D.供试品+杂质混合溶液 3
0
注:1.对氨基酚;2.对乙酰氨基酚;3.杂质 B;4.杂质 A;5.杂质 D;6.
0 10 20 30 40 50 60 70 80
未知杂质;7.杂质 F;8.羟苯甲酯;9.对氯苯乙酰胺;10.羟苯乙酯;11.羟 t,min
苯丙酯(下同) D.氧化破坏溶液
0.020 2
Note:1. p-aminophenol;2. paracetamol;3. impurity B;4. impurity
A;5. impurity D;6. unknown impurity;7. impurity F;8. methyl hydroxy- 0.015
benzoate;9. p-chloroacetanilide;10. ethyl hydroxybenzoate;11. propyl
AU 0.010
hydroxybenzoate(same as below)
0.005
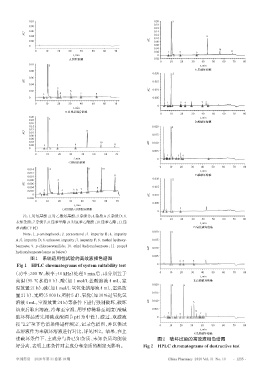
图1 系统适用性试验的高效液相色谱图
3 4 5
Fig 1 HPLC chromatograms of system suitability test 0
(功率:300 W,频率:40 kHz)处理 5 min 后,再分别置于 0 10 20 30 40 50 60 70 80
t,min
高温(95 ℃水浴 8 h)、酸(加 1 mol/L 盐酸溶液 4 mL,室 E.高温破坏溶液
0.020 2 4
温放置21 h)、碱(加1 mol/L 氢氧化钠溶液4 mL,室温放
0.015
置21 h)、光照(5 000 lx照射5 d)、氧化(加30%过氧化氢
溶液4 mL,室温放置24 h)等条件下进行强制破坏,破坏 AU 0.010 5
结束后取出溶液,冷却至室温,用甲醇稀释至刻度(酸碱 0.005 6
1 3 7
破坏样品需先用碱或酸调节 pH 为中性),滤过,取滤液 0
按“2.2”项下色谱条件进样测定,记录色谱图,并以供试 0 10 20 30 40 50 60 70 80
品溶液作为未破坏溶液进行对比,详见图2。结果,在上 t,min
F.光照破坏溶液
述破坏条件下,主成分与各已知杂质、未知杂质均能较 图2 破坏试验的高效液相色谱图
好分离,表明上述条件对主成分和杂质的测定无影响。 Fig 2 HPLC chromatograms of destructive test
中国药房 2020年第31卷第10期 China Pharmacy 2020 Vol. 31 No. 10 ·1235 ·