Page 54 - 《中国药房》2025年23期
P. 54
2.4 大鼠标准血浆样品和质控样品的配制 和日间精密度的 RSD 均小于 13%,准确度为 93.66%~
吸取大鼠空白血浆样品适量,加入100 μL利伐沙班 102.70%,符合2020年版《中国药典》生物样本的测定要
系列标准溶液和 200 μL 内标工作液,按“2.3”项下方法 求。结果见表1。
处理后,取上清液,即得系列标准血浆样品。另取“2.2” 2.8 基质效应考察
项下各质控工作液适量,同法配制定量下限和低、中、高 取大鼠空白血浆样品适量,共 6 份,按“2.3”项下方
质量浓度(0.66、1.64、160.00、1 000.00 ng/mL)的质控样 法处理后(不加内标工作液),即得空白基质;向空白基
品,备用。 质中加入定量下限和低、中、高质量浓度(0.66、1.64、
2.5 专属性考察 160.00、1 000.00 ng/mL)的利伐沙班质控工作液和内标
取大鼠空白血浆样品(不加内标)、定量下限质量浓 工作液,再按“2.1”项下色谱与质谱条件进样分析,获得
度质控样品、给药 1 h 后血浆样品(即“2.11.1”项下利伐 利伐沙班峰面积与内标峰面积比值(A);另用纯水替代
沙班单用组大鼠给予利伐沙班 1 h 后的血浆样品)各适 空白基质,其余操作同上,获得利伐沙班峰面积与内标
量,分别按“2.3”项下方法处理后,按“2.1”项下色谱与质 峰面积比值(B)。每个质量浓度均平行 6 份,基质效应
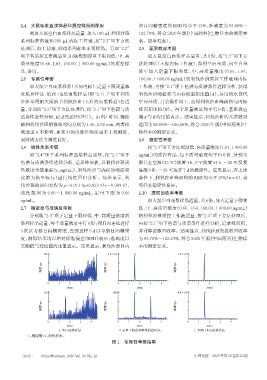
谱条件进样分析,记录色谱图(图1)。由图1可知,柳胺 用 A 与 B 的比值表示。结果显示,利伐沙班的基质效应
酚和利伐沙班的保留时间分别为1.46、1.50 min,两者检 范围为88.69%~106.16%,符合2020年版《中国药典》生
测通道互不影响,血浆中的内源性物质也不干扰测定, 物样本的测定要求。
表明该方法专属性良好。 2.9 稳定性考察
2.6 线性关系考察 按“2.4”项下方法配制低、高质量浓度(1.64、1 000.00
取“2.4”项下系列标准血浆样品适量,按“2.1”项下 ng/mL)的质控样品,每个质量浓度均平行 6 份,分别考
色谱与质谱条件进样分析,记录峰面积,以利伐沙班质 察其在室温(25 ℃)放置4 h、4 ℃放置24 h、-20 ℃反复
量浓度为横坐标(x,ng/mL)、利伐沙班与内标的峰面积 冻融3次、-20 ℃冻存7 d的稳定性。结果显示,在上述
比值为纵坐标(y)进行线性回归分析。结果显示,利 条件下,利伐沙班峰面积的 RSD 均小于 15%(n=6),表
伐沙班的回归方程为y=0.013 9x+0.023 9(r=0.999 0), 明样品稳定性良好。
线 性 范 围 为 0.66~1 000.00 ng/mL,定 量 下 限 为 0.66 2.10 提取回收率考察
ng/mL。 取大鼠空白血浆样品适量,共6份,加入定量下限和
2.7 精密度与准确度考察 低、中、高质量浓度(0.66、1.64、160.00、1 000.00 ng/mL)
分别取“2.4”项下定量下限和低、中、高质量浓度的 的利伐沙班质控工作液适量,按“2.3”项下方法处理后,
质控样品适量,每个质量浓度平行6份;同日内连续进样 再按“2.1”项下色谱与质谱条件进样分析,记录峰面积,
3 次以考察日内精密度,连续进样 3 d 以考察日间精密 并计算提取回收率。结果显示,利伐沙班的提取回收率
度,测得结果均以相对标准偏差(RSD)表示;准确度以 为94.71%~102.24%,符合2020年版《中国药典》生物样
实测值与理论值的比值表示。结果显示,利伐沙班日内 本的测定要求。
180 2.5×10 5 1 2.2×10 5 1
强度/cps 强度/cps 强度/cps
0 1 2 3 4 0 1 2 3 4 0 1 2 3 4
t/min t/min t/min
130 900 2 4.4×10 5 2
强度/cps 强度/cps 强度/cps
0 1 2 3 4 0 1 2 3 4 0 1 2 3 4
t/min t/min t/min
A.空白血浆样品 B.定量下限质量浓度质控样品 C.给药1 h后血浆样品
1:柳胺酚;2:利伐沙班。
图1 专属性考察结果
· 2932 · China Pharmacy 2025 Vol. 36 No. 23 中国药房 2025年第36卷第23期