Page 122 - 《中国药房》2025年22期
P. 122
IL-8
IL-6
TNF-α
mTOR复合物1
TNF-α
TNF-α
IL-1β
IL-8
IL-8 IL-6
IL-6 IL-8
IL-6
TNF-α
IL-13
TNF-α
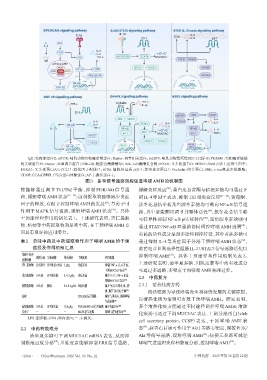
IgE:免疫球蛋白E;mTOR:哺乳动物雷帕霉素靶蛋白;Raptor:调节相关蛋白;mLST8:哺乳动物致死性SEC-13蛋白8;PRAS40:雷帕霉素敏感
的关联蛋白40;Deptor:双重调节蛋白;GSK-3β:糖原合酶激酶3β;IKK:IκB激酶复合物;FOXO:叉头框蛋白O;SPDEF:SAM点状上皮衍生因子;
FOXA3:叉头框蛋白A3;CCL11:趋化因子配体11;ECM:细胞外基质;ZO-1:紧密连接蛋白1;Occludin:闭合蛋白;JNK:c-Jun氨基末端激酶;
CHOP:CCAAT增强子结合蛋白同源蛋白;AP-1:激活蛋白-1。
图3 多种信号通路调控促进哮喘AMH的机制图
物能够通过调节 Th1/Th2 平衡、抑制 PI3K/Akt 信号通 缓解炎症反应 ;桑白皮总黄酮与桔梗多糖均可通过下
[26]
路,缓解哮喘AMH状态 [21—22] ;前胡提取物能够减少炎症 调 IL-4 等因子表达,抑制 Th2 型炎症反应 [27—28] ;紫菀酮、
因子的释放,有助于控制哮喘AMH的发展 ;葶苈子可 款冬花总倍半萜及鱼腥草素钠均可靶向 NF-κB 信号通
[23]
[24]
作用于 MAPK 信号通路,缓解哮喘 AMH 状态 。具体 路,其中紫菀酮可调节其整体活性 ,款冬花总倍半萜
[29]
干预途径和作用机制见表 1。上述研究表明,杏仁提取 可特异性抑制 NF-κB p65 核转位 ,而鱼腥草素钠则可
[30]
物、桔梗等中药提取物和单味中药,在干预哮喘AMH方 通过 STAT3/NF-κB 双通路协同调控哮喘 AMH 进展 ;
[31]
面具有良好的应用潜力。 黄芪的活性成分呈现多途径调控特征,其中黄芪多糖可
表1 单味中药及中药提取物作用于哮喘 AMH 的干预 通过抑制 IL-4 等炎症因子分泌干预哮喘 AMH 状态 ,
[32]
途径及作用机制汇总 黄芪皂苷Ⅱ则选择性阻断IL-21/STAT3信号通路活化以
单味中药/中 抑制哮喘 AMH 。具体干预途径和作用机制见表 2。
[33]
建模方法 实验动物 给药剂量 干预途径 作用机制
药提取物
杏仁提取物 LPS诱导 SPF级SD大鼠 3 g/kg 炎症反应 抑制TNF-α、IL-8升高, 上述研究表明,清半夏多糖、川陈皮素等中药有效成分
下调MUC5AC表达 [19] 可通过多通路、多靶点干预哮喘AMH病理过程。
当归提取物 OVA法 SPF级小鼠 8、4、2 g/kg 炎症反应 减少IL-13、TNF-α含量, 2.3 中药复方
抑制MUC5AC表达 [20]
桔梗提取物 OVA法 豚鼠 0.8、0.4 g/mL 氧化应激 减少氧自由基生成、释 2.3.1 清热化痰方药
放,调节Th1/Th2平衡 [21] 痰热壅肺为导致哮喘发生和持续发展的关键原因,
桔梗 - - - PI3K/Akt信号通路 减轻气道炎症,抑制哮喘
气道重塑 [22] 以清热化痰为治则可有效干预哮喘 AMH。研究表明,
前胡提取物 OVA法 SPF级大鼠 10.8 g/kg PI3K/Akt/NF-κB信号通路 减少炎症因子 [23] 多个清热化痰方能通过不同途径调控哮喘 AMH:清肺
葶苈子 - - - MAPK信号通路 抑制气道炎症反应 [24]
化痰汤可通过下调 MUC5AC 表达、上调分泌蛋白(club
LPS:脂多糖;OVA:卵白蛋白;-:未提及。
cell secretory protein,CCSP)表 达 ,干 预 哮 喘 AMH 状
[34]
2.2 中药有效成分 态 ;麻杏石甘汤可作用于Akt1等核心靶点,调控PI3K/
[35]
清半夏多糖可下调 MUC5AC mRNA 表达,从而抑 Akt 等信号通路,缓解哮喘 AMH ;桔梗元参汤可减轻
[36]
[25]
制黏液过度分泌 ;川陈皮素能够抑制 ERS 信号通路, 哮喘气道组织炎症和黏液分泌,控制哮喘AMH 。
· 2864 · China Pharmacy 2025 Vol. 36 No. 22 中国药房 2025年第36卷第22期