Page 58 - 《中国药房》2025年20期
P. 58
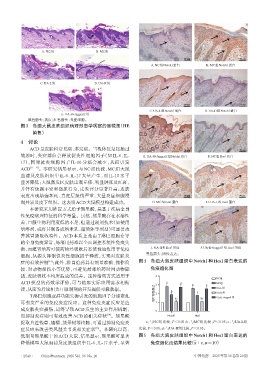
A. NC组 B. MC组
A. NC组Notch1蛋白 B. MC组Notch1蛋白
C. UA-L组 D. UA-H组
C. UA-L组Notch1蛋白 D. UA-H组Notch1蛋白
E. UA-H+Jagged1组
黑色箭头:表皮;红色箭头:炎症细胞。
图3 各组大鼠皮肤组织病理形态学观察的显微图(HE
染色)
4 讨论
ACD是皮肤科常见病、多发病。当机体反复接触过
敏原时,炎症部位会释放促炎性细胞因子(如 IL-6、IL- E. UA-H+Jagged1组Notch1蛋白 F. NC组Hes1蛋白
17),同时抗炎细胞因子 IL-10 分泌会减少,从而引发
ACD [11―12] 。本研究结果显示,与 NC 组比较,MC 组大鼠
血清及皮肤组织中 IL-6、IL-17 大量产生,而 IL-10 水平
显著降低;大鼠激发区皮肤出现丘疹、明显肿胀及红斑,
并伴有烦躁不安和搔抓行为,皮炎评分显著升高;皮肤
表皮出现结痂坏死、真皮层损伤严重、大量炎症细胞浸
润并累及皮下组织。这表明ACD大鼠模型构建成功。 G. MC组Hes1蛋白 H. UA-L组Hes1蛋白
本研究采用灌胃方式给予熊果酸,是基于疾病全身
性免疫病理特征的科学考量。虽然,熊果酸存在水溶性
差、口服生物利用度低的不足,但通过制剂技术(如使用
增溶剂,或将其制备成纳米乳、脂质体等剂型)可显著改
善其胃肠吸收特性。ACD 本质上是由 T 淋巴细胞介导
的全身免疫异常,局部用药难以全面调控系统性免疫失
衡,而灌胃给药可使药物经吸收后系统性地作用于免疫 I. UA-H组Hes1蛋白 J. UA-H+Jagged1组Hes1蛋白
细胞,从源头抑制促炎性细胞因子释放,实现对皮肤炎 黑色箭头:阳性表达。
[13]
症的有效控制 ;此外,灌胃给药具有剂量准确、操作简 图4 各组大鼠皮肤组织中 Notch1 和 Hes1 蛋白表达的
便、对动物损伤小等优势,可避免局部给药时因动物舔 免疫组化图
舐、皮肤吸收不均所造成的误差。这种给药方式适用于 4
NC组
ACD 模型的药效学评价,可与临床实际应用需求相衔 3 MC组
接,从而为后续相关口服制剂的开发提供可靠数据。 UA-L组
T淋巴细胞亚群功能失衡引发的细胞因子分泌紊乱 相对阳性表达 2 UA-H组
UA-H+Jagged1组
可引发严重的免疫炎症反应。这种免疫炎症反应是造 1
成皮肤炎症损伤,最终导致ACD发生的主要作用机制, 0
[14]
而抑制炎症则可有效改善 ACD 的相关症状 。熊果酸 Notch1 Hes1
提取自连钱草、越橘、熊果树等植物,可通过抑制免疫炎 a:与NC组比较,P<0.05;b:与MC组比较,P<0.05;c:与UA-L组
[15]
症反应来改善类风湿关节炎相关症状 。本研究以高、 比较,P<0.05;d:与UA-H组比较,P<0.05。
低剂量熊果酸干预ACD大鼠,结果显示,熊果酸可显著 图5 各组大鼠皮肤组织中 Notch1 和 Hes1 蛋白表达的
降低模型大鼠血清及皮肤组织中 IL-6、IL-17 水平,显著 免疫组化法结果比较(x±s,n=10)
· 2540 · China Pharmacy 2025 Vol. 36 No. 20 中国药房 2025年第36卷第20期