Page 31 - 《中国药房》2025年19期
P. 31
表2 各组小鼠海马组织中 Akt/Nrf2/HO-1 信号通路相
关蛋白表达量比较(x±s,n=3)
DAPI 组别 Nrf2/β-actin HO-1/β-actin p-Akt/β-actin p-Akt/Akt
Sham组 1.000±0.000 1.000±0.000 1.000±0.000 1.000±0.000
OVX组 0.159±0.026 a 0.331±0.021 a 0.906±0.018 0.800±0.019 a
ZSD-L组 0.517±0.078 b 0.468±0.015 b 1.267±0.020 1.099±0.024 b
Nrf2 a:与Sham组比较,P<0.01;b:与OVX组比较,P<0.01。
眠引起肝肾阴虚,导致内热上扰心神,从而出现心烦易
怒等情志失调;同时,阴虚火旺导致津液外泄,出现潮热
汗出。ZSD 在主“虚劳、虚烦不得眠”的酸枣仁汤基础
Merge 上,合主“烦热”“心中懊侬”的栀子豉汤,并配“疗虚清
热,补肾水真阴不足”之生地,全方共奏清火养阴、除烦
Sham组 OVX组 ZSD-L组
安神之效。
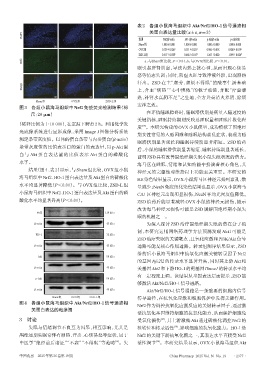
图3 各组小鼠海马组织中Nrf2免疫荧光检测结果(标
在评估睡眠障碍时,睡眠潜伏期是衡量入睡速度的
尺:20 μm)
关键指标,睡眠持续期则反映总睡眠量和睡眠片段化程
(稀释比例为1∶10 000),在室温下孵育2 h。利用化学发
[17]
度 。本研究构建的OVX小鼠模型,成功模拟了围绝经
光成像系统进行显影成像,采用 Image J 图像分析系统
期女性常见的入睡困难和睡眠结构紊乱症状,表现为睡
测定条带灰度值。以目的蛋白条带与内参蛋白(β-actin)
眠潜伏期显著延长和睡眠持续期显著缩短。ZSD 给药
条带灰度值的比值表示目的蛋白的表达量,以 p-Akt 蛋
后,小鼠的睡眠潜伏期显著缩短、睡眠持续期显著延长,
白与 Akt 蛋白表达量的比值表示 Akt 蛋白的磷酸化
证明ZSD具有改善围绝经期失眠小鼠失眠状况的潜力。
水平。
海马区在睡眠、情绪和认知功能中扮演着核心角色,其
结果(图4、表2)显示,与Sham组比较,OVX组小鼠 神经元的完整性对维持以上功能至关重要。本研究的
海马组织中Nrf2、HO-1蛋白表达量及Akt蛋白的磷酸化
HE染色结果显示,OVX小鼠海马区神经元排列紊乱、数
水平均显著降低(P<0.01)。与 OVX 组比较,ZSD-L 组 量减少;NeuN免疫组化染色结果也显示,OVX小鼠海马
小鼠海马组织中Nrf2、HO-1蛋白表达量及Akt蛋白的磷 CA1区神经元出现明显损伤,NeuN平均光密度值降低。
酸化水平均显著升高(P<0.01)。 ZSD 给药后能显著减轻 OVX 小鼠的神经元损伤,提示
改善海马神经元损伤可能是 ZSD 缓解围绝经期小鼠失
Nrf2 110 kDa
眠的机制之一。
β-actin 43 kDa 为深入探讨 ZSD 治疗围绝经期失眠的潜在分子机
制,本研究运用网络药理学方法预测发现 Akt1 可能是
HO-1 32 kDa
ZSD治疗失眠的关键靶点,且氧化应激和PI3K/Akt信号
β-actin 43 kDa 通路可能是核心作用通路。转录组测序结果显示,ZSD
给药后小鼠海马组织中抗氧化应激关键转录因子 Nrf2
Akt 56 kDa
的基因 Nfe2l2 的转录水平显著升高,同时其上游 Akt 相
β-actin 43 kDa 关基因Akt2和下游HO-1的靶基因Hmox1的转录水平均
有一定程度上调。该结果从基因表达层面提示,ZSD能
p-Akt 56 kDa
够激活Akt/Nrf2/HO-1信号通路。
β-actin 43 kDa Akt/Nrf2/HO-1 信号通路是一条重要的细胞内信号
Sham组 OVX组 ZSD-L组 传导途径,在抗氧化应激和细胞保护中发挥关键作用。
图4 各组小鼠海马组织中 Akt/Nrf2/HO-1 信号通路相
Nrf2作为调控抗氧化应激反应的关键转录因子,通过激
关蛋白表达的电泳图
活抗氧化基因维持细胞的抗氧化能力,从而保护细胞免
3 讨论 受氧化损伤 ,其上游激酶 Akt 通过磷酸化调控 Nrf2 的
[18]
失眠与情绪调节不良互为因果,相互影响,尤其是 核转位和转录活性 ,影响细胞的抗氧化能力。HO-1是
[19]
围绝经期失眠常伴有潮热、汗出、心烦易怒等症状,属于 Nrf2的关键下游抗氧化酶之一,其表达水平直接受Nrf2
[20]
[16]
中医学“绝经前后诸证”“不寐”“不得眠”等范畴 。失 活性调节 。本研究结果显示,OVX 小鼠海马组织 Akt
中国药房 2025年第36卷第19期 China Pharmacy 2025 Vol. 36 No. 19 · 2377 ·