Page 29 - 《中国药房》2025年19期
P. 29
素消毒,并用可吸收线和丝线缝合,最后涂抹红霉素软 2.2.5 神经元形态观察与NeuN蛋白免疫组化检测
膏 。Sham组小鼠不摘除卵巢,其余处理与各造模组小 末次给药后禁食 24 h,将小鼠(每组取 3 只)用 10%
[13]
鼠相同。术后进行动情周期检测,若阴道涂片显示无正 戊巴比妥钠完全麻醉后置于解剖台上,取出全脑用 4%
常动情周期变化或动情周期紊乱表明小鼠进入围绝经 多聚甲醛固定 24 h,制备小鼠海马石蜡切片(厚 4 μm),
[14]
期,提示造模成功 。本研究用于造模的50只小鼠均造 进行苏木精-伊红(HE)染色。将染色后的切片脱水透
模成功。 明,用中性树胶封片后,用 VS200 型数字切片扫描仪扫
2.2.3 给药 描并观察组织病理学变化。另取小鼠海马石蜡切片进
造模成功后,Sham 组和 OVX 组小鼠灌胃生理盐 行免疫组化染色,先用pH6.0的柠檬酸盐缓冲液在高温、
水;ZSD-L、ZSD-M、ZSD-H组小鼠分别灌胃ZSD水煎液 高压下进行抗原修复,然后用 5% 牛血清白蛋白在室温
11、22、33 g/kg,分别为临床等效剂量的1、2、3倍;ESZ组 下封闭30 min;加入NeuN一抗(稀释比例1∶10 000),在
小鼠灌胃右佐匹克隆1 mg/kg(以水为溶剂)。连续灌胃 4 ℃湿盒中孵育过夜;磷酸盐缓冲液(PBS)洗涤后,加入
3周,每天1次,灌胃体积均为10 mL/kg。 HRP 标记的山羊抗兔免疫球蛋白 G 二抗(稀释比例 1∶
2.2.4 睡眠潜伏期及睡眠持续期检测 200),在室温下孵育1 h后,DAB显色,苏木精复染,脱水
采用戊巴比妥钠睡眠协同实验检测。给药结束前 透明,并用中性树胶封片,显微镜观察并采集图像。采
1 d(灌胃结束1 h后),腹腔注射戊巴比妥钠(50 mg/kg), 用 Image J 软件对小鼠海马 CA1 区 NeuN 蛋白阳性表达
记录每只小鼠翻正反射消失和恢复的时间。睡眠潜伏 区域(呈黄褐色或棕黄色)进行光密度分析,并计算
期指从注射戊巴比妥钠到翻正反射消失的时间,睡眠持 NeuN的平均光密度值(平均光密度值=累积光密度值/
续期指翻正反射消失和恢复的时间间隔。采用 Graph‐ 区域面积×100%)。
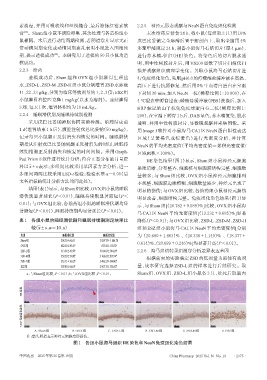
Pad Prism 8软件进行统计分析;符合正态分布的计量资 HE 染色结果(图 1)显示,Sham 组小鼠神经元细胞
料以 x±s 表示;多组间比较采用单因素方差分析,进一 条理清晰、分布整齐,细胞核与细胞膜结构完整,细胞数
步组间两两比较采用 LSD-t 检验;检验水准 α=0.05(后 量较多;与 Sham 组比较,OVX 组小鼠神经元细胞排列
文各指标的统计分析方法均同此处)。 不规整,细胞膜边缘模糊,细胞数量减少,神经元出现了
结果(表1)显示,与Sham组比较,OVX组小鼠的睡眠 明显的损伤;与OVX组比较,各给药组小鼠神经元损伤
潜伏期显著延长(P<0.01),睡眠持续期显著缩短(P<
明显改善,细胞结构完整。免疫组化染色结果(图 1)显
0.01);与OVX组比较,各给药组小鼠的睡眠潜伏期均显
示,与 Sham 组[(20.782±0.589)%]比较,OVX 组小鼠海
著缩短(P<0.01),睡眠持续期均显著延长(P<0.01)。
马 CA1 区 NeuN 平均光密度值[(13.232±0.685)%]显著
表1 各组小鼠的睡眠潜伏期和睡眠持续期测定结果比 降低(P<0.01);与OVX组比较,ZSD-L、ZSD-M、ZSD-H
较(x±s,n=10,s) 组和 ESZ 组小鼠海马 CA1 区 NeuN 平均光密度值[分别
组别 睡眠潜伏期 睡眠持续期 为(20.680±1.463)% 、(20.338±1.140)% 、(18.377±
Sham组 298.50±66.65 5 029.75±1 806.70 0.614)%、(20.699±0.246)%]均显著升高(P<0.01)。
OVX组 482.50±89.43 a 673.50±103.72 a
ZSD-L组 313.38±41.58 b 3 016.63±744.18 b 2.2.6 海马组织转录组测序分析差异表达基因
ZSD-M组 358.50±59.00 b 3 166.63±897.14 b 根据前面的实验确定 ZSD 的低剂量为最佳有效剂
ZSD-H组 353.13±56.62 b 3 496.25±384.42 b
ESZ组 307.00±66.65 b 2 967.75±786.52 b 量,故本研究选择 ZSD-L 组的样本进行后续研究。取
a:与Sham组比较,P<0.01;b:与OVX组比较,P<0.01。 Sham 组、OVX 组、ZSD-L 组小鼠各 3 只,处死后取脑内
HE染色
NeuN免疫组化染色
A. Sham组 B. OVX组 C. ZSD-L组 D. ZSD-M组 E. ZSD-H组 E. ESZ组
注:箭头所指表示神经元细胞变形损伤。
图1 各组小鼠海马组织HE染色和NeuN免疫组化染色结果
中国药房 2025年第36卷第19期 China Pharmacy 2025 Vol. 36 No. 19 · 2375 ·