Page 129 - 《中国药房》2024年23期
P. 129
1 肺部疾病应用纳米给药系统的挑战与机遇 术和材料,以优化肺部给药系统。通过合理的纳米给药
肺拥有3亿多个肺泡,肺泡被2层上皮细胞膜分隔, 系统设计和表面修饰,可以增强药物的稳定性和生物相
上皮细胞膜间密布大量毛细血管,形成了一个覆盖面积 容性,延长药物的肺部滞留时间和提高肺部对药物的吸
2
约为 100 m 的庞大网络,使得药物能够迅速被吸收,从 收效率,从而为实现肺部疾病的精准治疗提供新的机遇
[5]
而实现高浓度的肺部给药 。此外,下呼吸道有一层薄 (图2)。采用壳聚糖(chitosan,CS)类黏附性材料构建肺
薄的结缔组织,其中包含了纤维细胞、神经细胞、巨噬细 部纳米给药系统,可在纳米载体高比表面积的优势下,
胞和淋巴管等多种细胞和组织结构,使得肺和淋巴系统 增加药物在肺表面的黏附性,延长药物在肺部的滞留时
[6]
成为肺部给药的理想靶点 。 间,提高药物吸入转运效率 。针对蛋白、多肽类物质在
[6]
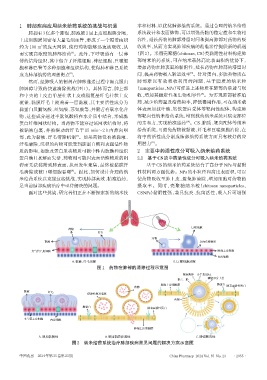
然而,经肺吸入的制剂在肺部递送过程中需克服由 肺部难以有效吸收利用的问题,基于脂质的纳米粒
肺屏障导致的快速清除挑战(图 1)。具体而言,肺上部 (nanoparticles,NPs)可促进上述物质在肺部的渗透与吸
[9]
和中央的上皮由单层柱状上皮或假复层纤毛柱状上皮 收,增加其稳定性和生物相容性 。为实现肺部精准给
覆盖,黏膜纤毛上覆盖着一层黏液,其主要活性成分为 药,减少给药量及给药频率,降低毒副作用,可在纳米载
黏蛋白及脯氨酸、丝氨酸、苏氨酸等,并附着有碳水化合 体表面加载叶酸、转铁蛋白受体等靶向性配体,构建肺
物,这些成分通过半胱氨酸桥在水介质中结合,形成黏 部靶向性纳米给药系统,增强载药纳米系统对病变部位
[10]
蛋白纤维网状结构。当药物不能穿过该网状结构时,将 的亲和力,实现精准递药 。CS、脂质、靶向配体等纳米
被黏液包裹,并被摆动的纤毛于 15 min~2 h 内推向咽 给药系统,可避免药物被黏液、纤毛和巨噬细胞清除,在
[7]
部,此为黏液、纤毛清除机制 。如果药物没有被黏液、 将中药活性成分制成肺部给药系统方面具有较好的应
[11]
纤毛清除,沉积的药物可能受到肺蛋白酶和表面活性物 用潜力 。
质的影响,如肽及蛋白质类物质可被中性内肽酶和组织 2 主要中药活性成分可吸入纳米给药系统
蛋白酶H水解而失活,药物则可能因表面活性物质的阻 2.1 基于CS的中药活性成分可吸入纳米给药系统
碍而无法黏附到肺表面,从而发生聚集,最终被黏膜纤 基于CS的纳米给药系统结合了高分子NPs与黏附
[8]
毛清除或被巨噬细胞吞噬 。因此,如何设计合理的纳 性材料两方面优势。NPs的小粒径和高比表面积,可以
米给药系统以克服这些挑战,实现肺部高效、精准给药, 使药物吸收至肺上皮,避免肺清除,增加细胞对药物的
是当前肺部疾病治疗中亟待解决的问题。 摄取率。同时,壳聚糖纳米粒(chitosan nanoparticles,
面对这些挑战,研究者们正在不断探索新的纳米技 CSNPs)黏附性强,兼具抗炎、抗菌活性,吸入后可增强
巨噬细胞
药物
纤毛
药物
黏液 表面活性物质
支气管上皮细胞 肺泡上皮细胞
内皮细胞
A.黏液、纤毛清除 B.巨噬细胞清除
图1 药物在肺部的清除过程示意图
靶向配体 小干扰RNA
磷脂双分子层
聚乙二醇
肺泡上皮细胞膜 糖蛋白
药物 肺表面活性蛋白
黏液 纤毛
促渗性纳米载体
药物
糖蛋白 肺表面活性蛋白
支气管上皮细胞 内皮细胞
肺泡上皮细胞膜
A.增加黏附性 B.增加黏膜渗透性 C.增强靶向性
图2 纳米给药系统治疗肺部疾病常见问题的解决方案示意图
中国药房 2024年第35卷第23期 China Pharmacy 2024 Vol. 35 No. 23 · 2955 ·