Page 55 - 《中国药房》2024年10期
P. 55
10 mPEG-PBLA胶束 2.2.6 纳米胶束体外释放研究
Cur/mPEG-PBLA胶束
8 首先,制备 Cur 对照品溶液:取 Cur 对照品适量,溶
强度/% 6 4 于 DMSO 中,再加水稀释至一定浓度,即得 Cur 对照品
2 溶液。然后,取 Cur 对照品溶液和 Cur/mPEG-PBLA 胶
0
1 10 100 1 000 10 000 束溶液各2 mL(两者质量浓度相同,以Cur计),各3份,
粒径/nm
A.粒径 B.显微形态(标尺200 nm) 分别装入透析袋中,并置于含释放介质[含0.5%吐温80
的pH7.4磷酸盐缓冲液(PBS)]25 mL的烧杯中,于37 ℃
80
Cur对照品 以 100 r/min振荡。分别于释放的 0、10、20、30 min 和 1、
Cur/mPEG-PBLA胶束
累积释放率/% 40 2、3、4、6、8、10、12、24、48 h 时取样 2 mL,并及时补充等
60
体积的新鲜释放介质。取样溶液按“2.2.4(1)”项下色谱
20
0 条件进样分析,记录峰面积并以外标法计算Cur含量,按
0 10 20 30 40 50
时间/h 下式计算每个时间点的累积释放率并绘制释放曲线:累
C.体外释放曲线(x±s,n=3) ( )
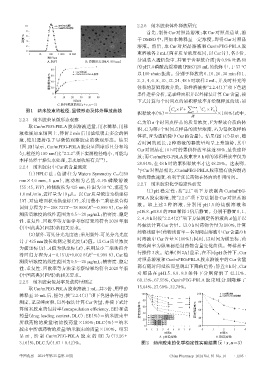
图1 纳米胶束的粒径、显微形态及体外释放曲线 C ´ V + ∑ i = n - 1 C ´ V 0
n
i
n = 1
积释放率(%)= W ×100%(式中,
2.2.3 纳米胶束显微形态观察
Cn为第 n 个时间点样品的质量浓度,V 为释放介质的体
取Cur/mPEG-PBLA胶束溶液适量,用水稀释,用移
积,Ci为第i个时间点样品的质量浓度,V0为每次取样的
液枪滴加至铜网上,停留 2 min 后用滤纸吸去多余的溶
体积,W为透析袋中Cur的含量)。结果(图1C)显示,随
液,使用透射电子显微镜观察胶束的微观形态。结果
着时间的延长,2 种溶液的释放量均呈上升趋势,其中
(图 1B)显示,Cur/mPEG-PBLA 胶束呈圆球形且分布均
Cur 对照品在 10 h 时的累积释放率接近 80%,呈快速释
匀,粒径约100 nm(比“2.2.2”项下实测粒径略小,可能与 放;而Cur/mPEG-PBLA胶束在8 h时的累积释放率仅为
[15]
本样品经干燥失水处理,亲水层收缩有关 )。
28.94%,在 48 h 时的累积释放率才达 48.25%。这表明,
2.2.4 纳米胶束中Cur的含量测定
与Cur对照品相比,Cur/mPEG-PBLA胶束能有效控制药
(1)HPLC 法:色谱柱为 Waters Symmetry C18 (250
物的释放速度,有利于延长药物在体内的作用时间。
mm×4.6 mm,5 μm),流动相为乙腈-0.1% 磷酸溶液
2.2.7 纳米胶束化学稳定性研究
(55∶45,V/V),检测波长为425 nm,柱温为30 ℃,流速为
(1)pH 稳定性:按“2.1”项下方法制备 Cur/mPEG-
1.0 mL/min,进样量为10 μL。以Cur质量浓度为横坐标
PBLA 胶束溶液,按“2.2.6”项下方法制备 Cur 对照品溶
(X)、对应峰面积为纵坐标(Y),采用最小二乘法拟合得
液。取上述 2 种溶液 ,分别用 pH1.5 的盐酸溶液和
2
回归方程为 Y=208 727X-78 088(R =0.999 9),Cur 检
pH6.8、pH8.0的PBS稀释1倍后静置。分别于静置0、1、
测质量浓度的线性范围为0.5~20 μg/mL;精密度、稳定
2、4、8 h时按“2.2.4(2)”项下方法测定各溶液的A值并以
性、重复性、回收率等方法学考察结果均符合 2020 年版
外标法计算 Cur 含量。以 0 h 时药物含量为 100%,计算
《中国药典》(四部)的相关要求。
药物残留率(药物残留率=各时间点溶液中Cur含量/0 h
(2)紫外-可见分光光度法:采用紫外-可见分光光度
时溶液中 Cur 含量×100%);同时,以时间为横坐标、药
计于425 nm波长处测定吸光度(A)值。以Cur质量浓度
物残留率为纵坐标绘制药物含量变化曲线。每样品平
为横坐标(X)、A 值为纵坐标(A),采用最小二乘法拟合
2
得回归方程为 A=0.151X+0.002 8(R =0.999 8),Cur 检 行操作 3 次。结果(图 2A)显示,在不同 pH 条件下,Cur
对照品溶液和 Cur/mPEG-PBLA 胶束溶液中的 Cur 含量
测质量浓度的线性范围为0.5~20 μg/mL;精密度、稳定
性、重复性、回收率等方法学考察结果均符合 2020 年版 都有随时间延长而呈现出下降的趋势;静置 8 h 时,Cur
《中国药典》(四部)的相关要求。 对照品在 pH1.5、6.8、8.0 条件下分别降解了 42.11%、
2.2.5 纳米胶束包封率及载药量测定 60.13%、67.55%,Cur/mPEG-PBLA 胶束则分别降解了
取Cur/mPEG-PBLA胶束溶液1 mL,共3份,用甲醇 15.04%、27.59%、32.78%。
稀释至10 mL后,摇匀,按“2.2.4(1)”项下色谱条件进样 100 100 Cur对照品溶液
Cur/mPEG-PBLA胶束溶液
测定,记录峰面积,以外标法计算Cur含量,并按下式计 80 80
算纳米胶束的包封率(encapsulation efficiency,EE)和载 药物残留率/% 60 药物残留率/% 60
药量(drug loading content,DLC):EE(%)=纳米胶束中 40 Cur/mPEG-PBLA胶束溶液(pH1.5)
Cur/mPEG-PBLA胶束溶液(pH6.8)
20 Cur/mPEG-PBLA胶束溶液(pH8.0) 40
所载药物的质量/初始投药量×100%;DLC(%)=纳米 Cur对照品溶液(pH1.5)
Cur对照品溶液(pH6.8)
0 Cur对照品溶液(pH8.0) 20
胶束中所载药物的质量/纳米胶束的质量×100%。结果 0 1 2 3 4 5 6 7 8 0 1 2 3 4
时间/h 时间/h
显 示 ,所 制 Cur/mPEG-PBLA 胶 束 的 EE 为(73.26± A. pH稳定性 B.热稳定性
3.16)%,DLC为(4.87±0.42)%。 图2 纳米胶束的化学稳定性实验结果(x±s,n=3)
中国药房 2024年第35卷第10期 China Pharmacy 2024 Vol. 35 No. 10 · 1205 ·