Page 51 - 《中国药房》2024年7期
P. 51
TLR4 90 kDa
NLRP3 115 kDa
GAPDH 36 kDa
p-NF-κB 65 kDa
50 μm 50 μm NF-κB 65 kDa
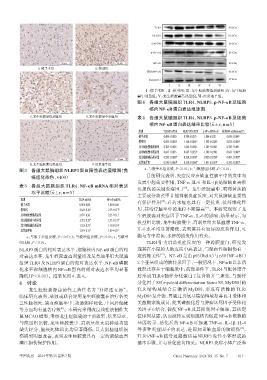
A.假手术组 B.模型组
核内NF-κB 65 kDa
histone H3 17 kDa
Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ Ⅵ
Ⅰ:假手术组 ;Ⅱ:模型组;Ⅲ:龙生蛭胶囊低剂量组;Ⅳ:龙生蛭胶
囊中剂量组;Ⅴ:龙生蛭胶囊高剂量组;Ⅵ:尼莫地平组。
图4 各组大鼠脑组织 TLR4、NLRP3、p-NF-κB 及细胞
核内NF-κB蛋白表达电泳图
50 μm 50 μm
C.龙生蛭胶囊低剂量组 D.龙生蛭胶囊中剂量组 表4 各组大鼠脑组织 TLR4、NLRP3、p-NF-κB 及细胞
核内NF-κB蛋白表达结果比较(x±s,n=5)
组别 TLR4/GAPDH NLRP3/GAPDH p-NF-κB/NF-κB 核内NF-κB/histone H3
假手术组 0.404±0.020 0.789±0.075 1.004±0.02 0.689±0.049
模型组 0.693±0.026 a 1.164±0.061 a 1.293±0.026 a 0.873±0.025 a
龙生蛭胶囊低剂量组 0.705±0.058 1.062±0.058 1.305±0.058 0.745±0.091
龙生蛭胶囊中剂量组 0.667±0.053 0.667±0.053 b 1.300±0.900 0.683±0.063 b
龙生蛭胶囊高剂量组 0.520±0.058 b 0.520±0.058 b 0.920±0.058 b 0.487±0.058 b
50 μm 50 μm
尼莫地平组 0.530±0.060 b 0.530±0.060 b 1.031±0.057 b 0.392±0.035 b
E.龙生蛭胶囊高剂量组 F.尼莫地平组
图3 各组大鼠脑组织NLRP3蛋白阳性表达显微图(免 a:与假手术组比较,P<0.01;b:与模型组比较,P<0.01。
疫组化染色,×400) 目前研究表明,炎症反应在缺血性脑卒中的发生与
发展中起重要作用,TNF-α、IL-6 和IL-1β是脑缺血再灌
表3 各组大鼠脑组织 TLR4、NF-κB mRNA 相对表达
[9]
注损伤的关键炎症因子 。龙生蛭胶囊中,君药黄芪的
水平比较(x±s,n=5)
主要成分黄芪甲苷能抑制炎症反应,对大鼠脑缺血损伤
组别 TLR4 mRNA NF-κB mRNA 有保护作用 ;君药水蛭也具有一定抗炎、抗纤维化作
[10]
假手术组 0.98±0.08 1.00±0.04
[11]
模型组 2.64±0.36 a 2.35±0.17 a 用,其治疗脑卒中的地位不断提高 。本研究观察了龙
龙生蛭胶囊低剂量组 2.47±0.26 2.25±0.13 生蛭胶囊对炎症因子TNF-α、IL-6的影响,结果显示,与
龙生蛭胶囊中剂量组 1.72±0.19 b 1.53±0.31 b 模型组比较,龙生蛭胶囊中、高剂量组大鼠血清TNF-α、
龙生蛭胶囊高剂量组 1.32±0.23 c 1.18±0.14 c
尼莫地平组 1.29±0.15 c 1.09±0.11 c IL-6 水平均显著降低,表明其具有较好的抗炎作用,可
a:与假手术组比较,P<0.01;b:与模型组比较,P<0.05;c:与模型 能与方中黄芪、水蛭的抗炎作用有关。
组比较,P<0.01。 TLR4 作为启动炎症反应的一种跨膜蛋白,研究发
NLRP3蛋白的相对表达水平、细胞核内NF-κB蛋白的相 现其在小鼠的大脑皮质中高表达,与缺血性脑损伤有一
[12]
对表达水平,龙生蛭胶囊高剂量组及尼莫地平组大鼠脑 定的相关性 。NF-κB是由p65(RelA)与p50(NF-κB1)
组织TLR4及NLRP3蛋白的相对表达水平、NF-κB磷酸 2个亚基组成的核转录因子,一般情况下,NF-κB以非活
化水平和细胞核内 NF-κB 蛋白的相对表达水平均显著 性形式存在于细胞质中;病理条件下,TLR4与配体结合
降低(P<0.01)。结果见图4、表4。 后形成 TLR4/髓样分化蛋白 2 复合物并二聚化,与髓样
4 讨论 分化因子88(myeloid differentiation factor 88,MyD88)的
龙生蛭胶囊源自清代王清任名方“补阳还五汤”。 TLR 结构域结合后激活 MyD88,形成有活性的 TLR/
临床研究表明,单独或联合应用龙生蛭胶囊在治疗各类 MyD88复合物,再通过其氨基端结构域招募IL-1受体相
急性脑梗死、缺血性脑卒中、动脉粥样硬化、中风后偏瘫 关激酶家族成员,使其磷酸化后与肿瘤坏死因子受体相
[8]
等方面均有显著疗效 。本研究采用改良线栓法制作大 关因子 6 结合,促使 NF-κB 及其抑制因子解聚,其核定
鼠MCAO模型,考察龙生蛭胶囊的干预效果,结果显示, 位序列暴露,从而被转运到细胞核内促进NF-κB依赖的
与模型组比较,龙生蛭胶囊中、高剂量组大鼠神经功能 基因转录,活化后的 NF-κB 可加速 TNF-α、IL-1β、IL-6
[13]
缺失评分、脑梗死体积比均显著降低,且大鼠脑组织损 等多种炎症因子的表达,进而加重缺血后的脑损伤 。
伤得到明显改善,表明龙生蛭胶囊具有一定的脑缺血再 TLR4/NF-κB 信号通路激活是 NLRP3 炎性小体形成的
灌注损伤保护作用。 基本步骤,并与活化密切相关。NLRP3炎症小体广泛参
中国药房 2024年第35卷第7期 China Pharmacy 2024 Vol. 35 No. 7 · 817 ·