Page 67 - 《中国药房》2024年2期
P. 67
50 25
b b b Ⅰ a Ⅰ
40 a a Ⅱ 20 a Ⅱ
a Ⅲ ( mmol/L ) 15 a Ⅲ
Ⅳ
Ⅳ
体重/g 30 Ⅴ 10 b b b b b b Ⅴ
20
10 空腹血糖/ 5
0 0
0周 4周 8周 0周 4周 8周
A.体重 B.空腹血糖
10 8 a A.对照组显微图 B.模型组显微图
a Ⅰ a Ⅰ
Ⅱ
8 a Ⅱ 6 a b Ⅲ
Ⅲ
24 h摄食量/g 6 4 a b b b b b b Ⅴ 24 h尿量/mL 4 2 b b b b b Ⅴ
Ⅳ
Ⅳ
0 2 0
0周 4周 8周 0周 4周 8周
C. 24 h摄食量 D. 24 h尿量
Ⅰ:对照组;Ⅱ:模型组;Ⅲ:阳性对照组;Ⅳ:GBE低剂量组;Ⅴ:
GBE高剂量组;a:与对照组比较,P<0.01;b:与模型组比较,P<0.01。 C.阳性对照组显微图 D. GBE低剂量组显微图
4
图1 GBE对DN模型小鼠体重、空腹血糖、摄食量及尿 a
量的影响(x±s,n=6) 3 b
表1 GBE对DN模型小鼠MCP-1、IL-12、IL-10水平的 肾损伤评分 2 b b
影响(x±s,n=6,pg/mL) 1
组别 MCP-1 IL-12 IL-10 0
Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ
对照组 14.39±1.63 41.85±3.19 297.01±25.28 E. GBE高剂量组显微图 F.各组肾损伤评分柱形图(x±s,n=6)
模型组 21.02±2.82 a 66.69±6.90 a 194.38±20.39 a Ⅰ:对照组;Ⅱ:模型组;Ⅲ:阳性对照组;Ⅳ:GBE低剂量组;Ⅴ:
阳性对照组 15.48±2.37 b 45.88±5.43 b 274.49±23.17 b
GBE高剂量组;黑色箭头:空泡;红色箭头:炎症细胞;a:与对照组比
GBE低剂量组 15.01±2.84 b 52.72±2.93 b 274.63±21.61 b
GBE高剂量组 13.98±2.39 b 45.19±5.33 b 296.25±22.57 b 较,P<0.01;b:与模型组比较,P<0.01。
图2 各组小鼠肾脏病理损伤显微图及肾损伤评分柱形
a:与对照组比较,P<0.01;b:与模型组比较,P<0.01。
图(HE染色)
3.3 GBE对DN模型小鼠肾功能相关指标的影响
与对照组比较,模型组小鼠血清BUN、Scr水平和双
侧肾脏质量与体重的比值均显著升高(P<0.01)。与模
型组比较,各药物组小鼠上述指标均显著降低(P<
0.01)。结果见表2。
表2 GBE对DN模型小鼠肾功能相关指标的影响(x±
A.对照组显微图 B.模型组显微图
s,n=6)
组别 BUN/(mmol/L) Scr/(μmol/L) 双侧肾脏质量与体重的比值/%
对照组 17.63±2.73 15.35±6.32 5.32±0.04
模型组 34.29±4.35 a 57.15±9.82 a 8.99±0.07 a
阳性对照组 22.46±3.34 b 35.98±12.29 b 5.83±0.11 b
GBE低剂量组 23.53±4.29 b 35.10±6.26 b 5.45±0.09 b
GBE高剂量组 21.69±3.06 b 28.43±7.38 b 4.19±0.06 b
a:与对照组比较,P<0.01;b:与模型组比较,P<0.01。 C.阳性对照组显微图 D. GBE低剂量组显微图
80
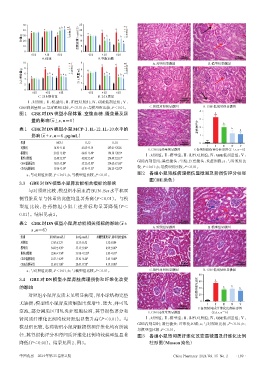
3.4 GBE 对 DN 模型小鼠肾脏病理损伤和纤维化改变 60 a
的影响 肾间质纤维化比例 40 b b b
对照组小鼠肾皮质未见明显病变,肾小球结构完整 20
无缺损;模型组小鼠肾皮质细胞出现增生、肥大,并可见 0 Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ
F.各组肾间质纤维化比例柱形图
空泡,部分间质区可见炎症细胞浸润,其肾损伤评分和 E. GBE高剂量组显微图 (x±s,n=6)
肾间质纤维化比例均较对照组显著升高(P<0.01)。与 Ⅰ:对照组;Ⅱ:模型组;Ⅲ:阳性对照组;Ⅳ:GBE低剂量组;Ⅴ:
GBE高剂量组;蓝色箭头:纤维化区域;a:与对照组比较,P<0.01;b:
模型组比较,各药物组小鼠肾脏损伤和纤维化均有所减
与模型组比较,P<0.01。
轻,其肾损伤评分和肾间质纤维化比例均较模型组显著 图3 各组小鼠肾间质纤维化改变显微图及纤维化比例
降低(P<0.01)。结果见图2、图3。 柱形图(Masson染色)
中国药房 2024年第35卷第2期 China Pharmacy 2024 Vol. 35 No. 2 · 189 ·