Page 49 - 《中国药房》2023年2期
P. 49
5 μm)为色谱柱;以 0.1% 三氟乙酸溶液(A)-甲醇(B)为 30 3 000
25
流动相进行梯度洗脱(0~15 min,98%A→80%A;15~ 20 mAU 2 000
30 min,80%A→98%A);流 速 为 0.5 mL/min;柱 温 为 mAU 15 1 000
10
5
30.0 ℃;检测波长为254 nm;进样体积为10 μL。 0 0
0 5 10 15 20 25 30 0 5 10 15 20 25 30
2.3.2 溶液的制备 (1)美洲大蠊提取物溶液:精密称 t/min t/min
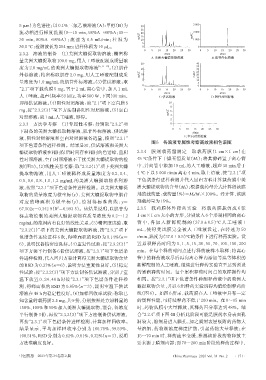
A.美洲大蠊提取物溶液 B.肌苷外标溶液
量美洲大蠊提取物100.0 mg,用人工唾液配制成质量浓
20 40
度为 2.0 mg/mL 的美洲大蠊提取物溶液 [6,11―12] 。(2)肌苷 15 35
30
外标溶液:精密称取肌苷 2.0 mg,用人工唾液配制成质 mAU 10 mAU 25
20
5 15
10
量浓度为 1.0 mg/mL 的肌苷外标溶液。(3)供试溶液:取 5
0 0
“2.1”项下载药膜 5 mg,置于 2 mL 离心管中,加入 1 mL 0 5 10 15 20 25 30 0 5 10 15 20 25 30
t/min t/min
人工唾液,超声(频率53 kHz,功率500 W,下同)30 min, C.供试溶液 D.阴性对照溶液
即得供试溶液。(4)阴性对照溶液:取“2.1”项下空白膜5 10
8
mg,按“2.3.2(3)”项下方法制备阴性对照溶液。(5)空白 mAU 6
对照溶液:取1 mL人工唾液,即得。 4
2
2.3.3 方法学考察 (1)专属性考察:分别取“2.3.2”项 0
0 5 10 15 20 25 30
下制备的美洲大蠊提取物溶液、肌苷外标溶液、供试溶 t/min
液、阴性对照溶液和空白对照溶液各适量,按照“2.3.1” E.空白对照溶液
图5 各溶液专属性考察高效液相色谱图
项下色谱条件进样检测。结果显示,供试溶液和美洲大
蠊提取物溶液在相同保留时间存在相同的色谱峰,且阴 2.3.4 膜剂载药量测定 取载药膜(1 cm×1 cm)在
性对照溶液、空白对照溶液不干扰美洲大蠊提取物的检 45 ℃条件下干燥至恒质量(M1 );将其剪碎置于离心管
测(图5)。(2)线性关系考察:取“2.3.2(1)”项下美洲大蠊 中,并向管中添加 10 mL 的人工唾液,超声 30 min 后于
提取物溶液,用人工唾液稀释成质量浓度为 0.2、0.4、 4 ℃下以 5 000 r/min 离心 4 min,取上清液,按“2.3.1”项
0.5、0.6、0.8、1.0、1.2 mg/mL 的美洲大蠊提取物系列溶 下色谱条件进样检测并代入回归方程计算载药膜中美
液,按照“2.3.1”项下色谱条件进样检测。以美洲大蠊提 洲大蠊提取物的含量(M2 );根据载药量公式计算得该膜
取物的质量浓度为横坐标(x)、美洲大蠊提取物中肌苷 剂的载药量:载药量(%)=M2/M1×100%。经计算,该膜
对应的峰面积为纵坐标(y),绘制得标准曲线:y= 剂载药量为15%。
2
67.502x-0.342 9(R =0.993 5)。该结果说明,以肌苷为 2.3.5 载药膜体外释药实验 将载药膜裁剪成 6 张
标志物绘制的美洲大蠊提取物在质量浓度为 0.2~1.2 1 cm×1 cm大小的方形,分别放入6个形制相同的离心
mg/mL的范围内有良好的线性关系。(3)精密度试验:取 管 中 ,各 加 入 新 鲜 配 制 的(37.0±0.5)℃ 人 工 唾 液 1
“2.3.2(1)”项下的美洲大蠊提取物溶液,按“2.3.1”项下 mL,使得受试膜完全被人工唾液没过,在转速为 50
色谱条件连续进样 6 次,得峰面积的 RSD 为 0.14%(n= r/min、温度为(37.0±0.5)℃的条件下进行释药实验。设
6),说明仪器精密度良好。(4)重复性试验:按“2.3.2(3)” 置累积释药时间为 0、1、5、15、30、50、70、100、150、200
项下方法平行制备 6 份供试溶液,按“2.3.1”项下色谱条 min。在每个释药时间点进行释药液样本取样:将离心
件进样检测,代入回归方程计算得美洲大蠊提取物含量 管中的释药液取尽后再向离心管内添加等温等体积的
的RSD为0.37%(n=6),说明方法重复性良好。(5)稳定 新鲜配制的人工唾液,继续进行释药实验直至达到预设
性试验:按“2.3.2(3)”项下方法制备供试溶液,分别于室 的累积释药时间。每个累积释药时间点的取样操作均
温下放置 0、24、48 h 时按“2.3.1”项下色谱条件进样检 相同。按“2.3.1”项下色谱条件检测释药液中的美洲大
测,得峰面积的 RSD 为 0.85%(n=3),说明室温下供试 蠊提取物含量,并以6组释药实验所得均值绘制释药曲
溶液在48 h内稳定性良好。(6)加样回收率试验:称取已 线(图 6)。如图 6 所示,载药膜在人工唾液中具有一定
知含量的载药膜2.5 mg,共9份,分别按照处方原料量的 的缓释性能,可持续释药不低于200 min。在0~15 min
150%、100%和50%加入美洲大蠊提取物,混合,各浓度 时,药物从膜中大量释放,其释药百分率达到 48%。结
平行制备 3 份,再按“2.3.2(3)”项下方法制备供试溶液, 合“2.2.4”项下图4B分析此阶段可能是膜剂本身表面孔
再按“2.3.1”项下色谱条件进样检测,计算加样回收率。 洞较大,溶剂易进入膜孔,加之膜剂表层吸附的药物大
结果显示,平均加样回收率分别为 100.75%、99.53%、 量溶解,药物顺浓度梯度扩散,引起药物大量释放;在
100.51%,RSD 分别为 0.82%、0.81%、0.32%(n=3),说明 15~70 min 时,释药速率变缓,推测该阶段药物释放主
方法准确度良好。 要来源于膜剂内部;而70~200 min阶段的释药过程中,
中国药房 2023年第34卷第2期 China Pharmacy 2023 Vol. 34 No. 2 · 171 ·