Page 29 - 《中国药房》2022年20期
P. 29
Li 的干燥根 ,因其产量和柴胡皂苷含量显著高于其他 min,55%A;8~9 min,55%A→70%A;9~10 min,70%A);
[4]
同属植物,且价格较低,常掺伪或混入北柴胡使用 。藏 柱温为40 ℃;流速为0.25 mL/min;进样量为5 μL。
[5]
柴胡与北柴胡、南柴胡等性状相似,化学成分基本一致, 2.1.2 质谱条件 采用电喷雾离子源,以多反应监测
考察到以感冒清热颗粒为代表的含柴胡中成药成分多 (multiple reaction monitoring,MRM)模式进行负离子扫
样 [6―7] ,故对掺伪筛查方法的专属性和准确性要求较高, 描。毛细管电压为 3 500 V;雾化器压力为 20 psi;干燥
而仅采用薄层色谱法、高效液相色谱(HPLC)法等手段 气温度为300 ℃,干燥气流速为10 L/min;鞘流气温度为
难以进行有效区分 [8―11] 。 350 ℃,鞘流气流速为 10 L/min;以 m/z 943.6→635.5(定
nepasaikosaponin K为五环三萜齐墩果烷型衍生物, 量离子对)、m/z 943.6→797.4(定性离子对)、m/z 943.6→
是藏柴胡特征性柴胡皂苷类成分 [12―13] 。本课题组前期 781.5(定性离子对)为特征离子对,碎裂电压均为 330
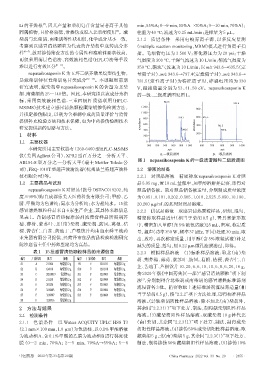
研究表明,藏柴胡中 nepasaikosaponin K 的含量为北柴 V,碰撞能量分别为 53、41、50 eV。nepasaikosaponin K
胡、南柴胡的25~140倍。因此,本研究拟以该成分为指 的一级、二级质谱图见图1。
标,采用高效液相色谱-三重四极杆质谱联用(HPLC-
943.6
943.6
MS/MS)技术建立感冒清热颗粒藏柴胡掺伪检测方法, 1 200 800
并拟定掺伪限度,以期为含柴胡中成药质量评价与监管 1 000 600 635.5
提供补充检验方法和技术保障,也为中药掺伪检测技术 800 979.7
600
研究提供新的思路与方法。 abundance 400 989.6 abundance 400 781.5
797.4
1 材料 200 200
1.1 主要仪器 0 0
900 920 940 960 980 1 000 600 700 800 900 1 000
本研究所用主要仪器有1260-6460型HPLC-MS/MS m/z m/z
仪(美国 Aglient 公司),XPR2 型百万分之一分析天平、 A.一级质谱图 B.二级质谱图
图1 nepasaikosaponin K的一级质谱图和二级质谱图
AB104-S 型万分之一分析天平(瑞士 Mettler Toledo 公
司),FRQ-1010T型超声波清洗器(杭州法兰特超声波科 2.2 溶液的制备
技有限公司)等。 2.2.1 对照品溶液 精密称取 nepasaikosaponin K 对照
1.2 主要药品与试剂 品5.05 mg,置10 mL量瓶中,加甲醇溶解并定容,即得对
nepasaikosaponin K 对照品(批号 DSTAC019202,纯 照品储备液。取对照品储备液适量,分别制成质量浓度
度≥98%)购自成都乐美天医药科技有限公司;甲醇、乙 为0.051、0.101、0.202、0.505、1.010、2.525、5.050、10.100、
腈、甲酸均为色谱纯;氨水为分析纯;水为超纯水。15批 20.200 μg/mL的系列对照品溶液。
感冒清热颗粒样品来自6家生产企业,其具体来源信息 2.2.2 供试品溶液 取感冒清热颗粒样品,研细,混匀,
见表 1。自制感冒清热标准汤剂流浸膏样品所需荆芥 精密称取样品适量(相当于柴胡 0.5 g),置具塞锥形瓶
穗、薄荷、紫苏叶、北(南)柴胡、藏柴胡、防风、葛根、桔 中,精密加入甲醇(含5%浓氨试液)25 mL,密塞,称定质
梗、苦杏仁、白芷、苦地丁、芦根饮片均由山东舜王城药 量,超声(功率350 W,频率37 kHz,下同)处理30 min,取
业集团有限公司提供,经菏泽市食品药品检验检测研究 出,放冷,再次称定质量,用甲醇(含 5% 浓氨试液)补足
院沙启营主任中药师鉴定均为真品。 减失的质量,摇匀,用0.22 μm微孔滤膜滤过,即得。
表1 15批感冒清热颗粒样品的来源信息 2.2.3 模拟样品溶液 (1)标准样品溶液:取北(南)柴
编号 厂家代码 批号 规格 编号 厂家代码 批号 规格 胡、荆芥穗、薄荷、紫苏叶、防风、葛根、桔梗、苦杏仁、白
S1 A 211106 每袋装12 g S9 F 3210317 每袋装12 g 芷、苦地丁、芦根饮片10、20、6、6、10、10、6、8、6、20、16 g,
S2 B 634118 每袋装12 g S10 F 3210318 每袋装12 g
S3 C 20210819 每袋装6 g S11 F 3210903 每袋装12 g 按2020年版《中国药典》(一部)“感冒清热颗粒”项下制
S4 D 211138 每袋装12 g S12 F 3210904 每袋装12 g 法 ,分别制得含北柴胡或南柴胡的感冒清热标准汤剂
[1]
S5 E 201234 每袋装12 g S13 F 3210905 每袋装12 g 流浸膏各3批。精密称取上述标准汤剂流浸膏适量(相
S6 F 3210605 每袋装12 g S14 F 3210906 每袋装12 g
S7 F 3210907 每袋装12 g S15 F 3210604 每袋装12 g 当于柴胡0.5 g),按“2.2.2”项下方法处理,即得标准样品
S8 F 3210316 每袋装12 g 溶液。(2)缺柴胡阴性样品溶液:除不加北(南)柴胡外,
2 方法与结果 其余同“2.2.3(1)”项下处方、制法,制得缺柴胡阴性样品
2.1 检测条件 溶液。(3)藏柴胡阳性样品溶液:取藏柴胡 10 g 替代北
2.1.1 色谱条件 以 Waters ACQUITY UPLC HSS T3 (南)柴胡,其余同“2.2.3(1)”项下处方、制法,制得藏柴
(2.1 mm×100 mm,1.8 μm)为色谱柱,以0.1%甲酸溶液 胡阳性样品溶液。(4)掺伪50%藏柴胡阳性样品溶液:取
为流动相A、含0.1%甲酸的乙腈为流动相B进行梯度洗 藏柴胡5 g,北(南)柴胡5 g,其余同“2.2.3(1)”项下处方、
脱(0~2 min,70%A;2~5 min,70%A→55%A;5~8 制法,制得掺伪50%藏柴胡阳性样品溶液。(5)掺伪10%
中国药房 2022年第33卷第20期 China Pharmacy 2022 Vol. 33 No. 20 ·2455·