Page 74 - 《中国药房》2022年13期
P. 74
0.6
盐酸麻黄碱 0.5
0.4
0.3
盐酸伪麻黄碱
0.2
0.1
盐酸麻黄碱+盐酸伪麻黄碱
S6 S9 S11 S19 S28 S32 S14 S18 S36 S27 S21 S22 S7 S24 S38 S16 S20 S25 S40 S17 S8 S2 S29 S30 S10 S34 S26 S33 S1 S23 S4 S37 S31 S35 S15 S3 S13 S39 S41 S5 S12
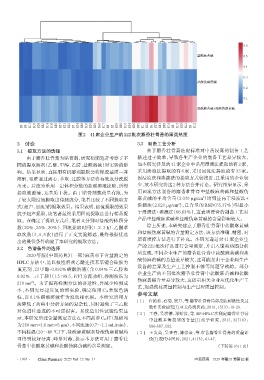
图2 41家企业生产的222批次麝香壮骨膏的聚类热图
3 讨论 3.3 制备工艺分析
3.1 提取方法的选择 由于麝香壮骨膏法定标准对中药浸膏的制备工艺
由于麝香壮骨膏为贴膏剂,研究初期笔者考察了不 描述过于简单,导致各生产企业的制备工艺差异较大,
同的提取溶剂(乙醚、甲醇、乙腈、盐酸溶液)对实验的影 如本研究涉及的41家企业中采用浸渍法提取的有2家,
响。结果显示,直接用有机溶剂提取会将橡胶基质一并 采用渗漉法提取的有 6 家,采用回流法提取的有 33 家。
溶解,很难通过离心、萃取、过膜等方法将有效成分洗脱 因浸渍法和渗漉法的提取方式较接近,且采用的企业较
出来。后改为采用一定体积分数的盐酸溶液提取,所得 少,故本研究将这2种方法合并讨论。研究结果显示,采
提取液澄清,无基质干扰。由于贴膏剂载药量有限,为 用回流方法制备的麝香壮骨膏中盐酸麻黄碱和盐酸伪
2
了较大限度地提取出待测成分,笔者比较了不同提取方 麻黄碱的平均含量(3.030 μg/cm)均明显高于浸渍法+
2
式(超声、回流)的提取效果。结果表明,回流提取的效果 渗漉法(2.623 μg/cm),且含量的 RSD(55.37%)明显小
优于超声提取,故笔者最终采用回流提取法进行样品提 于浸渍法+渗漉法(66.63%),这表明浸膏的制备工艺对
取。在确定了提取方式后,笔者又分别对盐酸的体积分 产品中盐酸麻黄碱和盐酸伪麻黄碱的含量影响较大。
综上所述,本研究建立了麝香壮骨膏中盐酸麻黄碱
数(20%、25%、30%)、回流提取时间(1、2、3 h)、乙醚萃
和盐酸伪麻黄碱的含量测定方法,该方法准确、精密,对
取次数(3、4、5 次)进行了正交实验筛选,最终根据优选
出的最佳条件确定了本研究的提取方法。 原有质控方法进行了补充。本研究通过对 41 家企业生
产的 222 批次样品进行含量测定,并引入聚类热图分析
3.2 色谱条件的选择
后发现,不同企业生产的麝香壮骨膏中盐酸麻黄碱和盐
2020 年版《中国药典》(一部)麻黄项下含量测定的
酸伪麻黄碱的总量差异较大,这可能是由于企业间生产
HPLC 方法中,是以极性溶剂乙醚连接苯基键合硅胶为
设备的差异及生产工艺控制不够等问题导致的。部分
填充剂,以甲醇-0.092%磷酸溶液(含 0.04%三乙胺和
企业生产的不同批次麝香壮骨膏中盐酸麻黄碱和盐酸
0.02%二正丁胺)(1.5 ∶ 98.5,V/V)为流动相,检测波长为
伪麻黄碱含量差异较大,这提示相关企业应优化生产工
210 nm 。为了提高检测方法的普适性,并减少检测成
[5]
艺,加强药材质量控制与生产过程质量控制。
本,本研究经过反复的预实验,确定使用 C18常规色谱
柱,以 0.1%磷酸溶液作为流动相水相。本研究所用方 参考文献
[ 1 ] 许艳茹,石菊,展月,等.麝香壮骨膏局部皮肤刺激性及过
法降低了药典中分析方法的复杂性,同时避免了三乙胺
敏性实验研究[J].亚太传统医药,2019,15(3):18-20.
对色谱柱造成的不可逆损害。系统适用性试验结果显
[ 2 ] 王春,吴世德,郑贻霞,等. RP-HPLC法测定麝香壮骨膏
示,本研究所建含量测定方法在不同品牌C18柱(规格均 中盐酸苯海拉明的含量[J].药学研究,2013,32(10):
为250 mm×4.6 mm×5 μm)、不同流速(0.7~1.1 mL/min)、 586-587,592.
不同柱温(20~40 ℃)下,盐酸麻黄碱和盐酸伪麻黄碱均 [ 3 ] 王发英,吴查青,陈张金,等.市售麝香壮骨膏的质量评
可得到较好分离,峰形对称,提示本方法可用于麝香壮 价[J].现代中医药,2021,41(5):41-47.
骨膏中盐酸麻黄碱和盐酸伪麻黄碱的含量测定。 (下转第1611页)
·1604 · China Pharmacy 2022 Vol. 33 No. 13 中国药房 2022年第33卷第13期