Page 21 - 《中国药房》2021年20期
P. 21
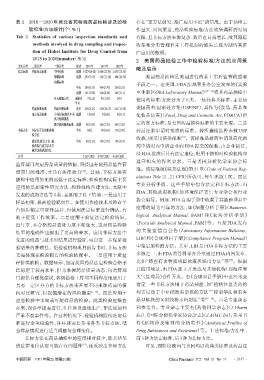
表 2 2018-2020 年湖北省药检院药品抽检涉及的检 存在“重方法研究、推广应用不足”的情况。由于抽检工
验标准/方法统计[个(%%)] 作量大、时间紧迫,药品检验标准/方法收集调研的时间
Tab 2 Statistics of various inspection standards and 有限,且非标方法来源复杂、数量也日益增长,故其跟踪
methods involved in drug sampling and inspec- 收集和分类管理日常工作机制的缺失已成为制约其推
tion of Hubei Institute for Drug Control from 广应用的瓶颈。
2018 to 2020[number(%%)] 2 美国药品抽检工作中检验标准/方法的应用策
方法分类 二级分类 三级分类 形式 2018年 2019年 2020年 略及启示
法定标准 国家药品标准 中国药典 成册 2 027(64.00)2 604(52.74)2 453(52.54)
部颁标准 成册 239(7.55) 552(11.18) 484(10.36) 美国药品抽检是美国进行药品上市后监管的重要
局颁标准 手段之一。在美国,FDA 法规事务办公室发布的《实验
单页 296(9.35) 434(8.79) 385(8.25)
成册 161(5.08) 234(4.74) 145(3.11) 室手册》(ORA Laboratory Manual) [14-15] 将其药品抽检中
补充检验方法 成册及 7(0.22) 95(1.92) 0(0) 使用的标准/方法分为了 6 类:一是药典类标准,主要是
单页
药品核准标准 药品注册标准 单页 258(8.15) 520(10.53) 621(13.30) 美国药典/国家处方集(USP/NF),其作为《食品、药品和
地方药品标准 中药材标准及中药 成册 1(0.03) 3(0.06) 8(0.17) 化妆品法案》(Food,Drug and Cosmetic Act,FD&CA)指
饮片炮制规范
医疗机构制剂标准 成册 98(3.09) 266(5.39) 243(5.20) 定的官方标准,是美国药品抽检标准的主要来源。二是
非标方法 国家局下发的推荐检 单页 0(0) 34(0.69) 135(2.89) 药品注册申请时批准的标准。若所抽检品种未被 USP
验方法
[16]
收载,则采用该类标准 。该标准是新药申请及简化新
探索性研究方法、检 单页 80(2.53) 195(3.95) 195(4.18)
验机构自建方法及文 药申请时由申请企业向 FDA 提交的标准,由企业制订,
献发表的成熟方法
经FDA批准后具有法定地位,但用于抽检时检验机构应
合计 3 167(100) 4 937(100) 4 669(100)
遵守相应的保密要求。三是美国分析化学家协会标
监管部门判定药品质量的依据,须经国务院药品监督管
准。该标准被《联邦法规》第21章(Code of Federal Reg-
[11]
理部门的批准,才具有法律效力 。目前,非标方法在
ulations Title 21,21 CFR)所认可,每年出版 1 次。四是
抽检中应用的比例远低于法定标准,检验机构实际主要
专业分析手册。这些手册中包含法定和非标方法,由
应用的是探索性研究方法、检验机构自建方法、文献中
FDA、其他政府机构(如环境保护署)、专业学会和行业
发表的成熟方法等3类,主要用于以下情境:一是应用于
协会编写。例如,FDA自编手册中收载了其抽检项目中
样品初筛,提高检验靶向性。如使用快检技术及筛查平
应用的最为可靠的方法,如《细菌分析手册》(Bauterio-
台初步锁定可疑样品后,再使用法定标准进行确认,有
logical Analytical Manual,BAM)和《农药分析手册》
助于提高工作效率。二是应用于验证法定检验结果。
近年来,不合格药品查处力度不断加大,这对药品检验 (Pesticide Analytical Manual,PAM)等。五是 FDA 发布
结果的准确性也提出了更高的要求。应用非标方法中 的实验室信息公告(Laboratory Information Bulletins,
先进的仪器与技术对结果进行验证,可以进一步保证检 LIB)和《合规项目手册》(Compliance Program Manual)
验结果的准确性。但检验机构出具报告书时,非标方法 中指定的检测方法。其中,LIB是FDA非标方法的主要
无需体现在检验报告的检验依据中。三是应用于质量 来源之一,由FDA监管科学办公室通过FDA内网发布,
[17]
评价类抽检。数据显示,当前我国药品法定检验合格率 比如“筛查有害物质残留的液质联用方法”等 。根据
已稳定于较高水平,但为掌握药品质量动态,向监管部 其应用场景,由 FDA 独立开发或与其他机构(如海洋和
门提供合理化建议,各级抽检工作均不同程度地运用了 大气管理局)合作开发。各《合规项目手册》中也经常会
具有一定区分力的非标方法来开展不同来源药品的横 指定一些非标方法用于药品抽检,如“检测沙坦类药物
向对比研究,以挖掘潜在的风险隐患 [1,12] 。四是应用于 和雷尼替丁中亚硝胺类杂质的方法”“控制华法林有害
应急检验中未知或可疑样品的检验。此类检验应稽查 晶型转换的X射线粉末衍射法”等 [18-19] 。六是专业杂志
办案、投诉举报而进行,往往涉及违规生产、非法添加和 和参考书。专业杂志主要有《药物科学杂志》(J Pharm
严重不良事件等。在这种情况下,检验机构除按法定标 Sci)、《国际分析化学家协会杂志》(J AOAC Int);参考书
准进行全项检验外,往往还需要参考各类非标方法,结 有《原料药及辅料的分析特性》(Analytical Profiles of
合样品情况进行适当调整与合理变化。 Drug Substances and Excipients)等。上述标准/方法中,
非标方法在药品抽检中的应用相对较少,除其结果 前3种为法定标准,后3种为非标方法。
[13]
的法律地位认定可能存在问题外 ,还反映出非标方法 可见,现阶段我国与美国均以药典类标准及药品注
中国药房 2021年第32卷第20期 China Pharmacy 2021 Vol. 32 No. 20 ·2447 ·