Page 72 - 《中国药房》2021年3期
P. 72
溶解并定容,得川芎嗪对照品贮备液。分别精密量取 2.3 川芎嗪脂质体制备工艺考察
0.05、0.10、0.15、0.20、0.25、0.30 mL 对照品贮备液置于 2.3.1 单因素试验 以包封率为指标,按“2.2”项下方法
10 mL量瓶中,加甲醇定容,制成系列对照品溶液;摇匀, 考察药脂比(1 ∶ 5、1 ∶ 10、1 ∶ 15、1 ∶ 20,m/m)、孵育温度
各取1 mL,以0.22 µm微孔滤膜滤过后取续滤液10 µL, (25、35、45、55 ℃)、孵育时间(10、20、30、40 min)、硫酸
按上述色谱条件进样测定,记录峰面积。以峰面积(Y) 铵溶液浓度(0.1、0.2、0.3、0.4 mol/L)、卵磷脂与胆固醇质
对川芎嗪质量浓度(X)进行线性回归,得回归方程为Y= 量比(1 ∶ 1、2 ∶ 1、3 ∶ 1、4 ∶ 1)、磷脂质量分数(0.8%、1.0%、
13 532X-10 531(R =0.999 5)。结果表明,川芎嗪的质 1.2%、1.5%)、超声功率(300、400、500、600 W)和超声时
2
量浓度在 5.08~30.48 µg/mL 范围内与其峰面积线性关 间(2、4、6、8 min)等因素对川芎嗪脂质体包封率的影
系良好。 响[包封率(%)=W 包封/W 总量×100%,式中 W 包封为被脂质
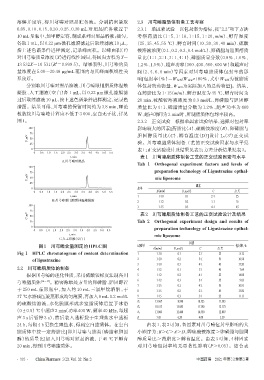
分别取川芎嗪对照品溶液、川芎嗪眼用脂质体温敏 体包封的药物量,W 总量为实际加入的总药物量]。结果,
凝胶、人工泪液(空白)各 1 mL,以 0.22 µm 微孔滤膜滤 在药脂比为 1 ∶ 15(m/m)、孵育温度为 45 ℃、孵育时间为
过后取续滤液10 µL,按上述色谱条件进样测定,记录色 20 min、硫酸铵溶液浓度为 0.3 mol/L、卵磷脂与胆固醇
谱图。结果可得,川芎嗪的保留时间约为 3.8 min,理论 质量比为 4 ∶ 1、磷脂质量分数为 1.2%、超声功率为 400
板数按川芎嗪峰计算应不低于3 000,空白无干扰,详见 W、超声时间为2 min时,所制脂质体包封率较高。
图1。 2.3.2 正交试验 根据单因素试验结果,选择对包封率
100 影响较大的因素[药脂比(A)、硫酸铵浓度(B)、卵磷脂与
75 4
mV 50 胆固醇质量比(C)、孵育温度(D)]设计 L9 (3)正交试
U,
25 验。川芎嗪脂质体制备工艺的正交试验因素与水平见
0 表1;正交试验设计及结果见表2;方差分析结果见表3。
0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5
t,min 表1 川芎嗪脂质体制备工艺的正交试验因素与水平
A.川芎嗪对照品
Tab 1 Orthogonal experiment factors and levels of
100
75 preparation technology of Ligustrazine opthal-
mV 50
U, mic liposome
25
因素
0 水平
0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 A(m/m) B,mol/L C D,℃
t,min 1 1∶10 0.1 2∶1 25
B.川芎嗪眼用脂质体温敏凝胶 2 1∶12 0.2 3∶1 35
100
3 1∶15 0.3 4∶1 45
75
mV 50 表2 川芎嗪脂质体制备工艺的正交试验设计及结果
U,
25 Tab 2 Orthogonal experiment design and results of
0 preparation technology of Ligustrazine opthal-
0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5
t,min mic liposome
C.人工泪液(空白)
因素
图1 川芎嗪含量测定的HPLC图 试验号 包封率,%
A(m/m) B,mol/L C D,℃
Fig 1 HPLC chromatogram of content determination 1 1∶10 0.1 2∶1 25 8.12
of ligustrazine 2 1∶10 0.2 3∶1 35 16.58
3 1∶10 0.3 4∶1 45 17.20
2.2 川芎嗪脂质体的制备 4 1∶12 0.1 3∶1 45 7.64
根据川芎嗪的理化性质,采用硫酸铵梯度法制备川 5 1∶12 0.2 4∶1 25 14.88
6 1∶12 0.3 2∶1 35 9.03
芎嗪脂质体 [16-17] 。精密称取处方量的卵磷脂、胆固醇置
7 1∶15 0.1 4∶1 35 10.91
于 250 mL 茄形瓶中,加入约 10 mL 三氯甲烷溶解,于 8 1∶15 0.2 2∶1 45 13.82
37 ℃水浴减压旋蒸形成均匀薄膜,再加入8 mL 0.2 mol/L 9 1∶15 0.3 3∶1 25 11.15
13.967 8.890 10.323 11.383
的硫酸铵溶液,水化脱膜形成多室脂质体后置于冰浴 K1
K2 10.517 15.093 11.790 12.173
(0±0.5)℃中超声2 min(功率400 W,频率40 kHz,每超
K3 11.960 12.460 14.330 12.887
声 3 s 后暂停 3 s),然后装入透析袋于生理盐水中透析 R 3.45 6.20 4.00 1.50
24 h,每隔4 h更换生理盐水,得到空白脂质体。在空白 由表1、表2可知,各因素对川芎嗪包封率影响的大
脂质体中按一定药脂比[即川芎嗪与脂类(磷脂和胆固 小顺序为:B>C>A>D,即硫酸铵浓度>卵磷脂与胆固
醇)的质量比]加入川芎嗪对照品溶液,于 45 ℃下孵育 醇质量比>药脂比>孵育温度。由表 3 可知,4 种因素
20 min,得到川芎嗪脂质体。 对川芎嗪包封率均无显著性影响(P>0.05)。结合表
·322 · China Pharmacy 2021 Vol. 32 No. 3 中国药房 2021年第32卷第3期