Page 40 - 202007
P. 40
醛麻醉大鼠,行胆管插管 。待大鼠清醒后,灌胃给予 动相为0.03%三氟乙酸水溶液-甲醇-乙腈溶液(66∶21∶13,
[14]
黄芩苷溶液[168 mg/kg,根据黄芩苷在茵栀黄软胶囊(主 V/V/V);流速为3 mL/min;柱温为40 ℃;检测波长为275
要活性成分为黄芩苷)中的用量换算而得]。持续收集 nm;进样量为40 µL。
大鼠24 h的胆汁,作为胆汁样品1,备用。取100 μL大鼠 2.2.2 黄芩苷代谢物的分离纯化 取 5 只大鼠,经水合
胆汁样品 1 于 5 mL 的离心管中,加入 0.5 mol/L 盐酸溶 氯醛麻醉后,同“2.1.3”项下方法麻醉、插管,待大鼠清醒
液 50 μL,涡旋混合 30 s,加入乙酸乙酯 2 mL,振荡 10 后,灌胃给予黄芩苷溶液(400 mg/kg,根据前期实验中大
min进行萃取,在4 ℃下以4 000 r/min离心10 min后,取 鼠的最大耐受剂量换算而得,为增加胆汁中代谢物含量
上清液于 40 ℃下氮气吹干,加甲醇 100 μL 复溶,再在 所以增加了灌胃剂量)。持续收集大鼠 48 h 的胆汁,作
4 ℃下以12 000 r/min离心10 min后,取上清液,备用。 为胆汁样品 2,于-20 ℃储存,备用。每次取 100 µL 胆
2.1.4 黄芩苷胆汁代谢物初步分析 取大鼠空白胆汁、 汁样品 2,加入 0.5 mol/L 盐酸 50 µL 涡旋混合 40 s,再加
大鼠空白胆汁+黄芩苷对照品、大鼠灌胃给药后的胆汁 2 mL 乙酸乙酯,振荡萃取 10 min 后,在 4 ℃下以 4 000
各适量,按“2.1.3”项下方法处理后,再按“2.1.1”项下色 r/min离心10 min,取上清液于氮气下吹干。重复上述操
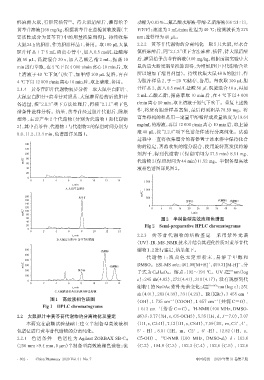
谱条件进样分析。结果,黄芩苷经过胆汁代谢后,除原 作,将所有胆汁样品富集,最后得到粗品 78.59 mg。将
型外,主要产生 2 个代谢物(分别为代谢物 1 和代谢物 富集得到的粗品用一定量甲醇稀释成质量浓度为19.64
mg/mL的溶液,再以12 000 r/min离心10 min后,取上清
2),其中黄芩苷、代谢物1与代谢物2的保留时间分别为
液 40 µL,按“2.2.1”项下色谱条件进行分离纯化。试验
8.0、11.2、13.4 min,色谱图详见图1。
过程中一直将收集馏分的容器置于冰水浴中保持化合
140 物的稳定,再将收集的馏分混合,使用旋转蒸发仪将溶
120
100 剂挥干,得到代谢物 1(保留时间为 37.5 min)8.51 mg、
mAU 80 代谢物 2(保留时间为 44 min)11.52 mg。半制备型高效
60
40 液相色谱图详见图2。
20
0
0 2 4 6 8 10 12 14
1 500
t,min
A.大鼠空白胆汁 1 000
mAU
180 黄芩苷 500
160 黄芩苷 代谢物1 代谢物2
140
120 0 0 5 10 15 20 25 30 35 40 45
mAU 100 t,min
80
60 图2 半制备型高效液相色谱图
40
20 Fig 2 Semi-preparative HPLC chromatograms
0
0 2 4 6 8 10 12 14
t,min 2.2.3 黄 芩 苷 代 谢 物 的 结 构 鉴 定 采 用 紫 外 光 谱
B.大鼠空白胆汁+黄芩苷对照品
(UV)、IR、MS、NMR技术并结合其理化性质对黄芩苷代
600 谢物1、2进行鉴定,结果如下。
代谢物1
500
代 谢 物 1:淡 黄 色 无 定 形 粉 末 ,易 溶 于 甲 醇 和
400
+
-
mAU 300 代谢物2 DMSO。ESI-MS m/z:461.08[M+H] ,459.31[M-H] ,分
200 黄芩苷 MeOH
子式为 C22H20O11。熔点:192~194 ℃。UV λ max nm(log
100
ε):245 sh(4.02),272(4.41),310(4.17);没有观察到代
0
0 2 4 6 8 10 12 14
λ
MeOH+AlCl 3
t,min 谢物 1 的 NaOAc 紫外光谱变化; max nm(log ε):251
C.大鼠灌胃给药后的胆汁样品溶液
sh(4.01),283(4.39),331(4.23)。IR(KBr):3 455 cm -1
图1 高效液相色谱图
- 1
- 1
(OH),1 735 cm (COOH),1 657 cm (共轭 C=O),
Fig 1 HPLC chromatograms
1
- 1
1 613 cm (芳香 C=C)。 H-NMR(400 MHz,DMSO-
2.2 大鼠胆汁中黄芩苷代谢物的分离纯化及鉴定 d6)δ:3.77(3H,s,C6-OCH3),5.35(1H,d,J=7.0),7.07
本研究在前期试验基础上建立半制备型高效液相 (1H,s,C3-H),7.12(1H,s,C8-H),7.59(3H,m,C3′,4′,
色谱法进行黄芩苷代谢物的分离纯化。 5′- H),8.01(2H,m,C2′,6′-H),12.82(1H,s,
2.2.1 色谱条件 色谱柱为 Agilent ZORBAX SB-C18 C5-OH)。 C-NMR(100 MHz,DMSO-d6 ) δ :163.6
13
(250 mm ×9.4 mm,5 µm)半制备型高效液相色谱柱;流 (C-2),104.8(C-3),182.3(C-4),152.6(C-5),132.6
·802 · China Pharmacy 2020 Vol. 31 No. 7 中国药房 2020年第31卷第7期