Page 84 - 202004
P. 84
变越明显;当RUE>1时,表示该组织对药物具有一定的 表明该组织对药物无摄取能力 [20-21] 。各指标计算公式如
摄取能力,提示药物具有一定的靶向性,而当RUE≤1则 下(式中,NPs、原料分别表示 AP-NPs 和 AP 原料药,下
30 血 同),结果见表5。
心
25 肝 ce=(cmax ) NPs/(cmax ) 原料 … … … … … … … … … … … ①
质量浓度,g/mL μ 15 肺 RUE=AUCNPs/AUC 原料 … … … … … … … … … … ②
脾
20
肾
由表 5 可见,AP-NPs 在血浆/组织样品中的 AUC、
脑
10
5 cmax与 AP 原料药比较,差异均有统计学意义(P<0.05)。
其中,AP-NPs 在血浆以及肝、脾、脑组织中的 RUE 均大
0
0.25 0.5 1 2 4 6 8 10 于1;血浆以及脾、脑组织的ce值也较高,但由于AP在上
时间,h
A. AP原料药 述组织中的 AUC 均低于肝脏(AP 原料药和 AP-NPs 在
30 血 肝脏中的 AUC 分别是血浆中的 3.46、4.66 倍,脾中的
心
25 肝 4.06、4.76 倍,脑中的 9.35、11.87 倍),故提示 AP 在肝组
质量浓度,g/mL μ 15 肺 织的积累量高于血浆以及脾、脑组织。
脾
20
肾
本研究就各组织对药物的摄取占比及其改变值进
脑
10
5 行了进一步分析,以考察药物在各个组织分布的比例
以及不同制剂在同一组织中分布的差异,进而评价组
0
0.25 0.5 1 2 4 6 8 10 织对不同制剂的摄取差异,相关计算公式如下,结果见
时间,h
B. AP-NPs 表 5。
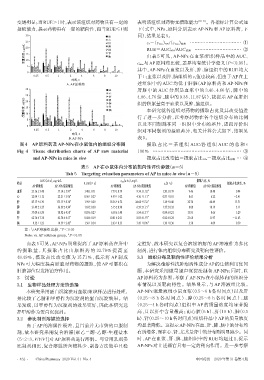
图4 AP原料药及AP-NPs在小鼠体内的组织分布图 摄 取 占 比 = 某 组 织 AUC/各 组 织 AUC 的 总 和 ×
Fig 4 Tissue distribution charts of AP raw material 100% … … … … … … … … … … … … … … … … … … … ③
and AP-NPs in mice in vivo 摄取占比改变值=摄取占比 NPs-摄取占比原料 … ④
表5 AP在小鼠体内分布的靶向性评价参数(n=5)
Tab 5 Targeting evluation parameters of AP in mice in vivo(n=5)
AUC(x±s),mg·h/L cmax (x±s),mg/L 摄取占比,%
样品 RUE(x±s) ce (x±s) 摄取占比改变,%
AP溶液组 AP-NPs混悬液组 AP溶液组 AP-NPs混悬液组 AP溶液组 AP-NPs混悬液组
血浆 25.16±3.48 37.14±5.93 * 1.48±0.31 7.79±0.79 9.34±1.32 * 1.20±0.39 9.46 10.40 0.94
心 22.94±3.12 22.21±3.96 * 0.96±0.27 4.99±1.02 4.36±1.13 * 0.87±0.18 8.63 6.22 -2.41
肝 87.17±6.39 173.17±8.38 * 1.99±0.29 18.36±4.72 24.68±5.32 * 1.34±0.40 32.78 48.49 15.71
脾 21.49±3.25 36.39±4.34 * 1.69±0.30 5.15±0.98 6.59±1.21 * 1.27±0.32 8.08 10.19 2.11
肺 37.09±5.38 30.92±4.58 * 0.83±0.27 6.58±1.40 5.54±1.17 * 0.84±0.21 13.95 8.66 -5.29
肾 62.76±7.38 42.74±4.57 * 0.68±0.19 10.01±2.01 8.03±1.97 * 0.82±0.24 23.60 11.97 -11.63
脑 9.32±1.23 14.59±2.42 * 1.56±0.34 2.63±0.53 3.43±0.96 * 1.30±0.36 3.50 4.09 0.59
*
注:与AP溶液组比较,P<0.05
*
Note:vs. AP solution group,P<0.05
由表 5 可见,AP-NPs 明显提高了 AP 原料药在肝中 定性好,故本研究以复合溶媒溶解的 AP 溶液作为参比
的 摄 取 量 ,其 摄 取 占 比 由 原 料 药 的 32.78% 提 高 至 制剂,进行体内组织分布研究及靶向性评价。
48.49%,摄取占比改变值为 15.71%,提示将 AP 制成 3.3 组织分布及靶向性评价结果分析
NPs 可大幅度提高肝脏对药物的摄取,使 AP 可累积在 为解决难溶性抗肿瘤活性成分AP的生物利用度问
肝脏部位以发挥治疗作用。 题,本研究采用微量超声沉淀法制备 AP-NPs;同时,以
3 讨论 AP原料药为参照,考察了AP-NPs在小鼠体内的组织分
3.1 生物样品处理方法的选择 布情况以及靶向特性。结果显示,与 AP 溶液组比较,
本研究采用蛋白沉淀法对血浆/组织样品进行处理, AP-NPs 混悬液组小鼠血浆(0.5~6 h 各时间点)以及肝
并比较了乙腈和甲醇作为沉淀剂的蛋白沉淀效果。结 (0.25~8 h 各 时 间 点)、脾(0.25~8 h 各 时 间 点)、脑
果发现,以甲醇作为沉淀剂的效果更好,因此本研究选 (0.25~4 h 各时间点)组织中 AP 的质量浓度均显著提
择甲醇作为蛋白沉淀剂。 高,且以肝中含量最高;而心脏(6 h)、肝(10 h)、肺(0.5
3.2 参比制剂溶媒的选择 h)、肾(0.25~10 h各时间点)组织样品中AP的质量浓度
由于 AP 的溶解性极差,且目前并无市售的口服制 均显著降低。这提示AP-NPs在血、肝、脾、脑中的分布均
剂,故本研究采用复合溶媒[聚乙二醇-乙醇-生理盐水 有所增多,而在心、肾,尤其是肾中的分布则明显减少。同
(5 ∶ 2 ∶ 3,V/V/V)]对AP原料药进行溶解。与常用乳剂参 时,AP 在血浆、肝、脾、脑组织中的 RUE 均超过 1,提示
比制剂相比,复合溶媒所含辅料少、制备方法简单且稳 AP-NPs对上述器官具有一定的靶向作用。进一步考察
·462 · China Pharmacy 2020 Vol. 31 No. 4 中国药房 2020年第31卷第4期