Page 84 - 中国药房2023年10期
P. 84
15%A→20%A;30~40 min,20%A→25%A;40~42 2.4.5 稳定性试验 取“2.1.2”项下供试品溶液(编号
min,25%A→35%A;42~50 min,35%A→40%A;50~55 S1),分别在室温下放置0、2、4、8、12、24 h时按“2.4.1”项
min,40%A→45%A;55~60 min,45%A→95%A;60~65 下色谱条件进样测定,记录峰面积。结果显示,毛蕊异
min,95%A;65~70 min,95%A→15%A;70~80 min, 黄酮葡萄糖苷、甘草苷、橙皮苷和甘草酸峰面积的 RSD
15%A);流速为 1.0 mL/min;柱温为 30 ℃;进样量为 10 分别为 1.12%、1.37%、0.65%、0.66%(n=6),表明供试品
μL;检测波长为 260 nm(0~29.5 min,毛蕊异黄酮葡萄 溶液在室温下放置24 h内稳定性良好。
糖苷)、276 nm(29.5~35 min,甘草苷)、283 nm(35~50 2.4.6 加样回收率试验 取同一批芪桂苓合剂(编号
min,橙皮苷)、251 nm(50~80 min,甘草酸)。该条件下 S1),共 6 份,每份 50 μL,以已知含量的 100% 加入混合
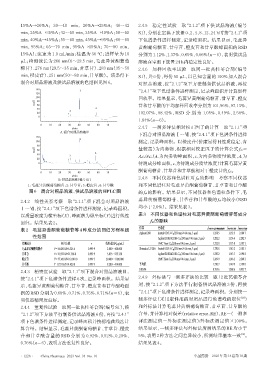
混合对照品溶液及供试品溶液的色谱图见图6。 对照品溶液,按“2.1.2”项下方法制备供试品溶液,再按
140
3 “2.4.1”项下色谱条件进样测定,记录峰面积并计算加样
120
100 回收率。结果显示,毛蕊异黄酮葡萄糖苷、甘草苷、橙皮
mAU 80 苷和甘草酸的平均加样回收率分别为101.96%、97.13%、
60
40 2 4
20 1 102.07%、98.42%,RSD 分 别 为 1.05%、0.49%、2.56%、
0
1.84%(n=6)。
0 10 20 30 40 50 60 70
t/min 2.4.7 一测多评法相对校正因子的计算 取“2.1.1”项
A.混合对照品溶液Ⅳ 下混合对照品溶液Ⅰ~Ⅶ,按“2.4.1”项下色谱条件进样
120
3
100 测定,记录峰面积。以橙皮苷(价廉易得且性质稳定、含
80
mAU 60 量较高)为内参物,根据相对校正因子的计算公式 fs/i=
40 2 4 Asci/Aics (As为内参物峰面积,cs为内参物质量浓度,Ai为
20 1
0 待测成分峰面积,ci为待测成分质量浓度)计算毛蕊异黄
酮葡萄糖苷、甘草苷和甘草酸相对于橙皮苷的fs/i。
0 10 20 30 40 50 60 70
t/min 2.4.8 不同仪器和色谱柱对 fs/i的影响 考察不同仪器
B.供试品溶液(编号S1)
1:毛蕊异黄酮葡萄糖苷;2:甘草苷;3:橙皮苷;4:甘草酸 和不同色谱柱对毛蕊异黄酮葡萄糖苷、甘草苷和甘草酸
图6 混合对照品溶液、供试品溶液的HPLC图 的 fs/i的影响。结果显示,不同仪器和色谱柱条件下,毛
蕊异黄酮葡萄糖苷、甘草苷和甘草酸的 fs/i均较小(RSD
2.4.2 线性关系考察 取“2.1.1”项下混合对照品溶液
Ⅰ~Ⅶ,按“2.4.1”项下色谱条件进样测定,记录峰面积。 均小于2.0%)。结果见表3。
以质量浓度为横坐标(X)、峰面积为纵坐标(Y)进行线性 表3 不同仪器和色谱柱对毛蕊异黄酮葡萄糖苷等成分
回归。结果见表2。 fs/i的影响
仪器 色谱柱
表2 毛蕊异黄酮葡萄糖苷等4种成分的回归方程和线 f 橙皮苷/毛蕊异黄酮葡萄糖苷 f 橙皮苷/甘草苷 f 橙皮苷/甘草酸
Agilent 1260 Inertsil ODS-3-C 18 (250 mm×4.6 mm,5 μm) 1.258 5 1.132 5 2.184 7
性范围 Agilent ZORBAX SB-C 18 (150 mm×4.6 mm,5 μm) 1.282 2 1.156 6 2.202 3
待测成分 回归方程 r 线性范围/(μg/mL) YMC Triart-C 18 (250 mm×4.6 mm,5 μm) 1.272 8 1.175 8 2.193 7
毛蕊异黄酮葡萄糖苷 Y=14.430 0X+6.326 6 0.999 9 2.000~100.000 Shimadzu LC-20A Inertsil ODS-3-C 18 (250 mm×4.6 mm,5 μm) 1.270 8 1.145 2 2.183 3
甘草苷 Y=15.932 0X+21.786 0 0.999 9 5.075~253.750 Agilent ZORBAX SB-C 18 (150 mm×4.6 mm,5 μm) 1.270 2 1.143 3 2.194 8
橙皮苷 Y=17.342 0X+163.010 0 0.999 5 20.400~1 020.000 YMC Triart-C 18 (250 mm×4.6 mm,5 μm) 1.269 9 1.146 2 2.240 2
甘草酸 Y=8.357 6X+14.420 0 0.999 9 8.280~414.000 平均值 1.270 7 1.149 9 2.199 8
RSD/% 0.595 6 1.288 6 0.953 7
2.4.3 精密度试验 取“2.1.1”项下混合对照品溶液Ⅲ,
按“2.4.1”项下色谱条件进样 6 次,记录峰面积。结果显 2.4.9 外标法与一测多评法的比较 取 12 批芪桂苓合
示,毛蕊异黄酮葡萄糖苷、甘草苷、橙皮苷和甘草酸峰面 剂,按“2.1.2”项下方法平行制备供试品溶液 3 份,再按
积的RSD分别为0.68%、0.71%、0.75%、0.71%(n=6),表 “2.4.1”项下色谱条件进样测定,记录峰面积。分别按一
[13]
明仪器精密度良好。 测多评法(采用定性用的对照品进行色谱峰的定位 )
2.4.4 重复性试验 取同一批芪桂苓合剂(编号S1),按 和外标法计算毛蕊异黄酮葡萄糖苷、甘草苷、甘草酸的
“2.1.2”项下方法平行制备供试品溶液 6 份,再按“2.4.1” 含量,并计算相对误差(relative error,RE),RE=(一测多
项下色谱条件进样测定,记录峰面积并按标准曲线法计 评法测定值-外标法测定值)/外标法测定值×100%。
算含量。结果显示,毛蕊异黄酮葡萄糖苷、甘草苷、橙皮 结果显示,一测多评法与外标法所测结果的 RE 均小于
[14]
苷和甘草酸含量的 RSD 分别为 0.92%、0.52%、0.20%、 5%,表明2种方法之间差异较小,所测结果基本一致 。
0.76%(n=6),表明方法重复性良好。 结果见表4。
· 1226 · China Pharmacy 2023 Vol. 34 No. 10 中国药房 2023年第34卷第10期