Page 59 - 《中国药房》2022年7期
P. 59
复方丹参片低剂量组比较,复方丹参片中、高剂量组大 低(P<0.05)。
鼠血清中 TC、TG、Cr、BUN 水平均显著降低(P<0.05); 3.3 大鼠肾脏组织病理形态学观察结果
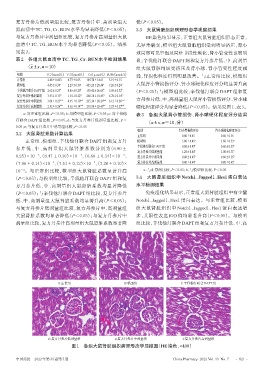
与复方丹参片中剂量组比较,复方丹参片高剂量组大鼠 HE染色结果显示,正常组大鼠肾脏组织形态正常,
血清中 TC、TG、BUN 水平均显著降低(P<0.05)。结果 无异常病变;模型组大鼠肾脏组织受到明显挤压,肾小
见表2。 球局部可见空泡及局灶节段性硬化,肾小管变性也较明
表2 各组大鼠血清中TC、TG、Cr、BUN水平检测结果 显;辛伐他汀联合DAPT组和复方丹参片低、中、高剂量
(x±±s,n=10) 组大鼠肾脏组织受挤压及肾小球、肾小管变性程度减
组别 TC/(mmol/L) TG/(mmol/L) Cr/(μmol/L) BUN/(mmol/L) 轻,肾损伤程度得到明显改善。与正常组比较,模型组
正常组 2.48±0.023 0.77±0.05 185.78±14.61 5.19±0.15
模型组 4.45±0.39 a 2.29±0.50 a 435.25±28.44 a 7.26±0.24 a 大鼠肾小管损伤评分、肾小球硬化程度评分均显著升高
辛伐他汀联合DAPT组 2.62±0.23 b 0.56±0.20 b 195.42±26.68 b 5.05±0.32 b (P<0.05);与模型组比较,辛伐他汀联合 DAPT 组和复
复方丹参片低剂量组 3.55±0.15 bc 1.34±0.22 bc 268.34±10.45 bc 6.78±0.14 bc
复方丹参片中剂量组 3.04±0.23 bcd 0.95±0.10 bcd 235.34±20.29 bcd 6.12±0.26 bcd 方丹参片低、中、高剂量组大鼠肾小管损伤评分、肾小球
复方丹参片高剂量组 2.52±0.26 bde 0.62±0.14 bde 210.90±26.49 bd 5.25±0.27 bde 硬化程度评分均显著降低(P<0.05)。结果见图1、表3。
a:与正常组比较,P<0.05;b:与模型组比较,P<0.05;c:与辛伐他 表 3 各组大鼠肾小管损伤、肾小球硬化程度评分结果
汀联合 DAPT 组比较,P<0.05;d:与复方丹参片低剂量组比较,P<
(x±±s,n=10,分)
0.05;e:与复方丹参片中剂量组比较,P<0.05
组别 肾小管损伤评分 肾小球硬化程度评分
3.2 大鼠肾脏系数计算结果
正常组 0.80±0.45 0.60±0.55
正常组、模型组、辛伐他汀联合 DAPT 组和复方丹 模型组 3.80±0.45 a 3.60±0.55 a
辛伐他汀联合DAPT组 0.80±0.45 b 0.60±0.55 b
参片低、中、高剂量组大鼠肾脏系数分别为(6.90±
复方丹参片低剂量组 1.20±0.44 b 1.00±0.71 b
- 2
- 2
0.25)×10 、(8.47±0.30)×10 、(6.60±0.34)×10 、 复方丹参片中剂量组 0.80±0.45 b 0.60±0.55 b
- 2
(7.96±0.14)×10 、(7.51±0.12)×10 、(7.20±0.10)× 复方丹参片高剂量组 0.80±0.44 b 0.80±0.45 b
-2
-2
10 。与正常组比较,模型组大鼠肾脏系数显著升高 a:与正常组比较,P<0.05;b:与模型组比较,P<0.05
-2
(P<0.05);与模型组比较,辛伐他汀联合 DAPT 组和复 3.4 大鼠肾脏组织中 Notch1、Jagged1、Hes1 蛋白表达
方丹参片低、中、高剂量组大鼠肾脏系数均显著降低 水平检测结果
(P<0.05);与辛伐他汀联合 DAPT 组比较,复方丹参片 免疫组化结果显示,正常组大鼠肾脏组织中有少量
低、中、高剂量组大鼠肾脏系数均显著升高(P<0.05); Notch1、Jagged1、Hes1 蛋白表达。与正常组比较,模型
与复方丹参片低剂量组比较,复方丹参片中、高剂量组 组大鼠肾脏组织中 Notch1、Jagged1、Hes1 蛋白表达增
大鼠肾脏系数均显著降低(P<0.05);与复方丹参片中 多,其阳性表达 IOD 值均显著升高(P<0.05)。与模型
剂量组比较,复方丹参片高剂量组大鼠肾脏系数显著降 组比较,辛伐他汀联合DAPT组和复方丹参片低、中、高
A.正常组 B.模型组 C.辛伐他汀联合DAPT组
D.复方丹参片低剂量组 E.复方丹参片中剂量组 F.复方丹参片高剂量组
图1 各组大鼠肾脏组织病理形态学显微图(HE染色,×400)
中国药房 2022年第33卷第7期 China Pharmacy 2022 Vol. 33 No. 7 ·821 ·