Page 53 - 《中国药房》2022年7期
P. 53
检验水准α=0.05。结果显示,FRL 的平均粒径和 Zeta 之间比较采用单因素方差分析,组间两两比较采用
电位分别为(172.70±3.76)nm和(-1.16±0.15)mV,RL Turkey 检验,检验水准α=0.05。结果,FCL 组细胞的绿
的平均粒径和 Zeta 电位分别为(169.10±4.15)nm 和 色荧光强度(134.89±17.61)显著高于 CL 组(22.30±
(-1.42±0.18)mV,2种叶酸脂质体间粒径和Zeta电位 10.62)和空白对照组(15.34±4.39)(P<0.01),表明细胞
差异均无统计学意义(P>0.05)。 对 FCL 的摄取量显著高于 CL。该结果提示,所制叶酸
2.3.2 包封率 参考文献[17-18]方法并加以调整后进 靶向阴离子脂质体可以有效地将药物递送到 HepG2 细
行测定。取5 nmoL anti-miR-221溶于250 µL水中,配成 胞内。
20 µmol/L的水溶液,作为母液。取母液分别制备成1.0、
0.8、0.5、0.4、0.25 µmol/L 5个浓度的水溶液,利用全波长
扫描式多功能读数仪在激发波长 493 nm、发射波长 518
nm条件下检测其荧光强度。以anti-miR-221浓度(x)为
横坐标、荧光强度(y)为纵坐标作图(图 1),并拟合得到
线性回归方程 y=168 676x-2 472.1(R =0.999 6)。结
2
果显示,anti-miR-221在上述检测浓度范围内,与其荧光
强度呈现出良好的线性关系。
20 μm 20 μm
200 000
150 000
荧光强度 100 000
50 000
0
0 0.5 1 1.5
浓度/(μmol/L)
20 μm
图1 anti-miR-221的标准曲线
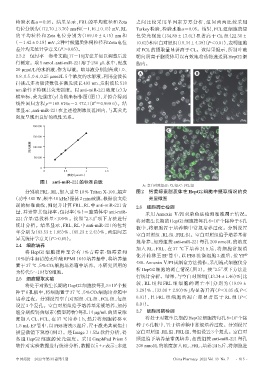
A:空白对照组;B:CL组;C:FCL组
分别取 FRL、RL,加入适量 10% Triton X-100,超声 图 2 钙黄绿素脂质体在 HepG2 细胞中摄取情况的荧
(功率480 W、频率40 kHz)振荡2 min破膜,根据前文绘 光显微图
制的标准曲线,测定并计算 FRL、RL 中 anti-miR-221 含 2.6 细胞凋亡检测
量,并计算其包封率:包封率(%)=脂质体中 anti-miR- 采用 Annexin Ⅴ/PI 双染色法检测细胞凋亡情况。
221 含量/总投料量×100%。按照“2.3.1”项下方法进行
将对数生长期的HepG2细胞按每孔8×10 个接种于6孔
5
统计分析。结果显示,FRL、RL 中 anti-miR-221 的包封
板中,将细胞置于培养箱中常规培养过夜。分别设置
率分别为(83.53±1.85)%、(85.23±2.43)%,两组间差 空白对照组、RL组、FRL组。空白对照组给予培养基常
异无统计学意义(P>0.05)。 规培养,加药组按 anti-miR-221 每孔 200 nmol/L 的浓度
2.4 细胞培养
加入 RL、FRL,在 37 ℃下培养 24 h 后,将细胞常规消
将 HepG2 细胞接种至含有 1%青霉素-链霉素和
10%胎牛血清的无叶酸RPMI 1640培养基中,将培养基 化并转移至 EP 管中,以 PBS 洗涤细胞 3 遍后,按 YF ®
488- Annexin Ⅴ/PI试剂盒方法操作,采用流式细胞仪分
置于 37 ℃、5%CO2细胞培养箱中培养。本研究所用的
析 HepG2 细胞的凋亡情况(图 3)。按“2.5”项下方法进
为传代5~10代的细胞。
2.5 细胞摄取实验 行统计分析。结果,与空白对照组[(13.34±1.46)%]比
较 ,RL 组 和 FRL 组 细 胞 的 凋 亡 率 [ 分 别 为(19.09 ±
5
将处于对数生长期的HepG2细胞按每孔5×10 个接
种于6孔板中,将细胞置于37 ℃、5%CO2细胞培养箱中 3.28)%、(33.08±2.90)%]均显著升高(P<0.05 或 P<
培养过夜。分别设置空白对照组、CL 组、FCL 组,每组 0.01),且 FRL 组细胞的凋亡率显著高于 RL 组(P<
设置3个复孔。空白对照组给予培养基常规培养,加药 0.01)。
组分别按钙黄绿素(模型药物)每孔 14 μg/mL 的质量浓 2.7 细胞周期检测
5
度加入 CL、FCL,在 37 ℃培养 1 h,然后将细胞转移至 将处于对数生长期的HepG2细胞按每孔8×10 个接
1.5 mL EP 管中,以 PBS 清洗 3 遍后,置于激光共聚焦扫 种于6孔板中,置于培养箱中常规培养过夜。分别设置
描显微镜下观察(图 2)。经 Image J 1.52a 软件分析,得 空白对照组、RL组、FRL组,每组设置3个复孔。空白对
各组 HepG2 细胞的荧光强度。采用 GraphPad Prism 5 照组给予培养基常规培养,加药组按 anti-miR-221 每孔
软件对实验数据进行统计分析,数据以 x±s 表示;多组 200 nmol/L的浓度加入RL、FRL,培养24 h后,将细胞进
中国药房 2022年第33卷第7期 China Pharmacy 2022 Vol. 33 No. 7 ·815 ·