Page 46 - 《中国药房》2022年1期
P. 46
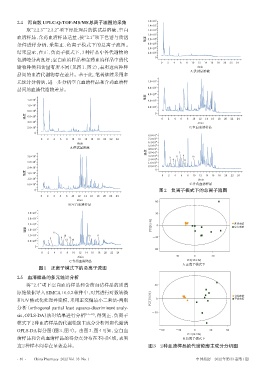
2.4 泻白散 UPLC-Q-TOF-MS/MS总离子流图的采集 1.6×10 7
1.4×10 7
取“2.2.3”“2.3.2”项下经处理后的供试品溶液、空白 1.2×10 7
1.0×10 7
血清样品、含药血清样品适量,按“2.1”项下色谱与质谱
强度 8.0×10 6
条件进样分析,采集正、负离子模式下的总离子流图。 6.0×10 6
4.0×10 6
结果显示,在正、负离子模式下,3 种样品中各代谢物的 2.0×10 6
0
色谱峰分离良好;空白血清样品和含药血清样品中的代
0 2 4 6 8 10 12 14 16 18 20 22 24
谢物种类和含量有所不同(见图1、图2),表明这两种样 t/min
A.供试品溶液
品间的血清代谢物存在差异。基于此,笔者继续采用多
元统计分析法,进一步分析空白血清样品和含药血清样 1.0×10 7
品间的血清代谢物差异。 8.0×10 6
6.0×10 6
强度
1.2×10 7 4.0×10 6
1.0×10 7
2.0×10 6
8.0×10 6
0
强度 6.0×10 6 0 2 4 6 8 10 12 14 16 18 20 22 24
4.0×10 6 t/min
2.0×10 6 B.空白血清样品
0
8.0×10 6
0 2 4 6 8 10 12 14 16 18 20 22 24 7.2×10 6
t/min 6.4×10 6
A.供试品溶液 5.6×10 6 6
4.8×10
强度 4.0×10 6 7
3.6×10 7 3.2×10 6 2 5 8 15
2.4×10 6 4 11
3.0×10 7 1.6×10 6
2.4×10 7 8.0×10 0 5
强度 1.8×10 7 0 2 4 6 8 10 12 14 16 18 20 22 24
1.2×10 7 t/min
6.0×10 6 C.含药血清样品
0 图2 负离子模式下的总离子流图
0 2 4 6 8 10 12 14 16 18 20 22 24
t/min
60
B.空白血清样品
3.6×10 7 30
3.0×10 7
2.4×10 7 PC2[9.5%] 0 含药血清
空白血清
强度 1.8×10 7 6
1.2×10 7 10 16 17 -30
3 9 13
6.0×10 6 1 12 14
0
-60
0 2 4 6 8 10 12 14 16 18 20 22 24
t/min -40 0 40
C.含药血清样品 PC1[18.1%]
A.正离子模式下
图1 正离子模式下的总离子流图
2.5 血清样品的多元统计分析
将“2.4”项下空白血清样品和含药血清样品的质谱 30
原始数据导入SIMCA 16.0.2软件中,对其进行对数转换 含药血清
和UV格式化处理并建模,采用正交偏最小二乘法-判别 PC2[10.5%] 0 空白血清
分析(orthogonal partial least squares-discriminant analy-
-30
sis,OPLS-DA)法对结果进行分析 [11-13] ,得到正、负离子
模式下2种血清样品的代谢轮廓主成分分析图和代谢谱
OPLS-DA得分图(图3、图4)。由图3、图4可知,空白血 -60 -30 0 30 60
PC1[14.9%]
清样品和含药血清样品的得分点分布在不同区域,表明 B.负离子模式下
这2种样本间存在显著差异。 图3 2种血清样品的代谢轮廓主成分分析图
·40 · China Pharmacy 2022 Vol. 33 No. 1 中国药房 2022年第33卷第1期