Page 30 - 《中国药房》2021年12期
P. 30
际操作的可控性,最终确定最优条件为萃取时间 36 线性回归,得回归方程为y=2 034.3x+32.3(r=0.999 0)。
min、盐浓度 11%、搅拌速度 800 r/min,并在此条件下平 结果表明,胡薄荷酮在质量浓度 0.05~5 μg/mL 范围内
行进行 6 次验证实验。结果显示,6 次平行验证实验的 与其峰面积呈良好的线性关系。
EF分别为88.5、93.0、88.4、92.2、90.6、91.1(RSD=2.1%,
90
n=6),与模型预测值(91.1)比较,偏差的绝对值低于
2.9%,说明该模型拟合结果准确、可靠。同时,分别取萃 60 胡薄荷酮
取前后的供试品溶液①(批号 20170524),分别按“2.2” mAU
30
项下色谱条件进样分析,记录色谱图。结果显示,经
HF-LPME 处理后的样品再经 HPLC 分析可表现出明显 0
的浓集和纯化效果,而仅采用 HPLC 法则无此优势。 0 5 10 15 20
t,min
HF-LPME 萃取前后样品中胡薄荷酮测定的 HPLC 图见 A.对照品溶液
图8。
80
120 60
mAU 40
90
mAU 60 20
0
30
0 5 10 15 20
0
t,min
0 5 10 15 20 B.基质溶液
t,min
120
A.供试品溶液①萃取前
90
120
mAU 60 胡薄荷酮
90
30
mAU 60 胡薄荷酮
0
30
0 5 10 15 20
0 t,min
C.供试品溶液①
0 5 10 15 20
t,min
600
B.供试品溶液①萃取后
图 8 HF-LPME 萃 取 前 后 样 品 中 胡 薄 荷 酮 测 定 的 400
HPLC图 mAU
200 胡薄荷酮
Fig 8 HPLC chromatograms of content determina-
tion of pulegone in sample before and after ex- 0
traction of HF-LPME 0 5 10 15 20
t,min
2.6 胡薄荷酮含量测定方法的建立及应用 D.供试品溶液②
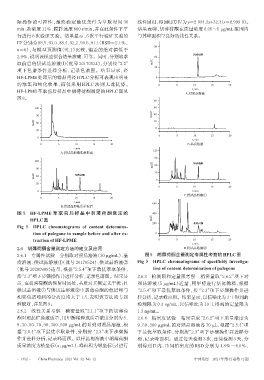
2.6.1 专属性试验 分别取对照品溶液(30 μg/mL)、基 图9 胡薄荷酮含量测定专属性考察的HPLC图
质溶液、供试品溶液①(批号 20170524)、供试品溶液② Fig 9 HPLC chromatograms of specificity investiga-
(批号 20200908)适量,根据“2.5.4”项下最优萃取条件, tion of content determination of pulegone
按“2.3”项下步骤操作并进样分析,记录色谱图。结果显 2.6.3 检测限和定量限考察 精密量取“2.6.2”项下对
示,在胡薄荷酮的保留时间处,基质对其测定无干扰;且 照品溶液(5 μg/mL)适量,用甲醇进行倍比稀释,根据
供试品溶液①与供试品溶液②中胡薄荷酮的色谱峰与 “2.5.4”项下最优萃取条件,按“2.3”项下步骤操作并进
相邻色谱峰间的分离度均大于 1.5,表明该方法的专属 样分析,记录峰面积。结果显示,以信噪比为3∶1得到的
性较好,详见图9。 检测限为 0.4 ng/mL,以信噪比为 10 ∶ 1 得到的定量限为
2.6.2 线性关系考察 精密量取“2.1.1”项下的胡薄荷 1.3 ng/mL。
酮对照品贮备液适量,用甲醇稀释成质量浓度分别为5、 2.6.4 精密度试验 精密量取“2.6.2”项下质量浓度为
9、30、50、70、90、300、500 μg/mL 的系列对照品溶液,根 9、50、300 μg/mL 的对照品溶液各 70 µL,根据“2.5.4”项
据“2.5.4”项下最优萃取条件,分别按“2.3”项下步骤操 下最优萃取条件,分别按“2.3”项下步骤操作并进样分
作并进样分析,记录峰面积。以样品相溶液中胡薄荷酮 析,记录峰面积。通过每天检测 3 次、连续检测 3 天,分
质量浓度为横坐标(x,μg/mL)、峰面积为纵坐标(y)进行 别得到日内、日间精密度的 RSD 分别为 1.8%~4.0%、
·1432 · China Pharmacy 2021 Vol. 32 No. 12 中国药房 2021年第32卷第12期