Page 54 - 《中国药房》2022年24期
P. 54
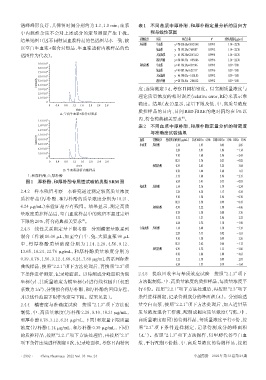
谱峰峰形良好,其保留时间分别约为 1.3、1.0 min;血浆 表1 不同基质中厚朴酚、和厚朴酚定量分析的回归方
中内源性杂质不会对上述成分的定量测定产生干扰。 程与线性范围
结果见图1(因不同种属血浆样品的色谱图基本一致,故 待测成分 基质 回归方程 R 2 线性范围/(μg/mL)
厚朴酚 牛血浆 y=70 030.68x+50 831.48 0.999 3 1.14~22.76
以空白牛血浆+混合对照品、牛血浆透析内液样品的色 兔血浆 y=78 193.29x+7 684.07 0.999 2 1.14~22.76
谱图作为代表)。 大鼠血浆 y=45 192.38x+22 431.12 0.999 4 1.14~22.76
透析外液 y=38 302.57x-4 959.86 0.999 6 1.14~22.76
9.0×10 6 2 和厚朴酚 牛血浆 y=41 136.29x+4 377.46 0.999 3 0.39~7.80
8.0×10 6
兔血浆 y=41 007.14x+6 217.17 0.999 6 0.39~7.80
7.0×10 6
6.0×10 6 大鼠血浆 y=46 390.03x-5 501.05 0.999 2 0.39~7.80
intensity 5.0×10 6 6 透析外液 y=20 736.81x-2 040.52 0.999 2 0.39~7.80
4.0×10
3.0×10 6 度;连续测定3 d,考察日间精密度。以实测质量浓度与
2.0×10 6 1
1.0×10 6 理论质量浓度的相对误差(relative error,RE)来表示准
0
0 0.4 0.8 1.2 1.6 2.0 2.4 2.8 确度。结果(表 2)显示,定量下限及低、中、高质量浓度
t/min 质控样品的日内、日间 RSD 和 RE 的绝对值均在 5% 以
A.空白牛血浆+混合对照品
[8]
2 内,符合药典相关要求 。
1.6×10 7
1.4×10 7 表2 不同血浆中厚朴酚、和厚朴酚定量分析的精密度
1.2×10 7 与准确度试验结果
1.0×10 7
intensity 8.0×10 6 6 血浆 待测成分 理论质量浓度/(μg/mL) 日内RSD(n=6)/% 日间RSD(n=3)/% RE(n=3)/%
6.0×10
4.0×10 6 1 牛血浆 厚朴酚 1.14 1.97 0.43 -2.05
2.28
3.81
-1.14
1.86
2.0×10 6
9.10 1.60 2.96 -2.43
0
0 0.4 0.8 1.2 1.6 2.0 2.4 2.8 18.21 2.76 0.23 -0.02
t/min 和厚朴酚 0.39 2.43 3.25 -3.04
B.牛血浆透析内液样品 0.78 1.44 2.68 -1.67
1:和厚朴酚;2:厚朴酚 3.12 1.60 2.96 -2.35
图1 厚朴酚、和厚朴酚专属性试验的典型SRM图 6.24 3.41 0.33 -0.05
兔血浆 厚朴酚 1.14 2.36 1.79 -2.24
2.4.2 样本残留考察 本研究通过测定较高质量浓度 2.28 4.28 1.17 -0.34
质控样品(厚朴酚、和厚朴酚的质量浓度分别为 18.21、 9.10 1.38 2.96 -0.70
18.21 2.58 0.99 -0.45
6.24 μg/mL)来验证是否有残留。结果显示,测定高质 和厚朴酚 0.39 2.22 1.90 -4.46
量浓度质控样品后,空白血浆样品中的残留不超过定量 0.78 1.30 0.88 -3.76
3.12 1.21 2.96 -2.32
下限的20%,符合药典相关要求 。 6.24 2.72 1.18 -1.90
[8]
2.4.3 线性关系和定量下限考察 分别精密量取系列 大鼠血浆 厚朴酚 1.14 2.40 1.30 -3.19
2.28 3.35 0.92 -1.65
混合工作液 10.00 μL,加至空白牛、兔、大鼠血浆 90 μL 9.10 1.38 0.99 -2.26
中,得厚朴酚质量浓度分别为 1.14、2.28、4.56、9.12、 18.21 2.62 0.64 -1.12
和厚朴酚 0.39 2.72 1.33 -3.86
13.65、18.24、22.76 μg/mL,和厚朴酚质量浓度分别为
0.78 1.86 1.00 -4.65
0.39、0.78、1.56、3.12、4.68、6.24、7.80 μg/mL 的系列标准 3.12 1.78 0.99 -2.87
6.24 1.37 0.19 -1.64
曲线样品,按照“2.2.1”项下方法处理后,再按照“2.3”项
下条件进样测定,记录峰面积。以待测成分峰面积为纵 2.4.5 提取回收率与基质效应试验 按照“2.1.3”项下
坐标(y)、其质量浓度为横坐标(x)进行线性回归(权重 方法配制低、中、高质量浓度的质控样品,每质量浓度平
2
系数为1/x),分别拟合得厚朴酚、和厚朴酚的回归方程, 行6份。按照“2.2.1”项下方法处理后,再按照“2.3”项下
并以线性范围下限作为定量下限。结果见表1。 条件进样测定,记录待测成分的峰面积(As )。分别取适
2.4.4 精密度与准确度试验 按照“2.1.3”项下方法配 量空白血浆,按照“2.2.1”项下方法处理后,加入适量某
制低、中、高质量浓度(厚朴酚 2.28、9.10、18.21 μg/mL, 质量浓度混合工作液,配制成相应质量浓度(与低、中、
和厚朴酚0.78、3.12、6.24 μg/mL,下同)和定量下限质量 高质量浓度相同)的待测样品,每质量浓度平行6份,按
浓度(厚朴酚 1.14 μg/mL、和厚朴酚 0.39 μg/mL,下同) 照“2.3”项下条件进样测定,记录待测成分的峰面积
的质控样品,按照“2.2.1”项下方法处理后,再按照“2.3” (As’)。按照“2.1.3”项下方法操作,以甲醇代替空白血
项下条件连续进样测定6次,记录峰面积,考察日内精密 浆,平行配制 6 份低、中、高质量浓度的待测样品,按照
· 2992 · China Pharmacy 2022 Vol. 33 No. 24 中国药房 2022年第33卷第24期