Page 125 - 《中国药房》2022年4期
P. 125
用药时的孕周或药物暴露时的孕周)、暴露药物及暴露 的某事件发生率及其 95%CI 上下限的原始结果分别用
时间、人免疫缺陷病毒(human immunodeficiency virus, p、ULP、LLP表示,转换后所得合并某事件的发生率及其
HIV)发生率、结局指标等。 95%CI 上下限分别用 pf、UL、LL 表示,pf=p/(1+p),
1.4 纳入文献质量评价 UL=ULP/(1+ULP ),LL=LLP/(1+LLP )。当纳入研究的
采用Cochrane系统评价员手册6.2版推荐的偏倚风 总例数≤3 时,考虑偏倚较大,遂进行敏感性分析;当总
险评估工具对纳入的RCT进行质量评价,包括随机分配 例数≤3 且事件发生数等于观察对象总例数时,该研究
方法、分配方案隐藏、盲法、结果数据的完整性、选择性 数据则不被纳入 Meta 分析 。采用χ 检验分析各研究
[11]
2
报告研究结果、其他偏倚来源,每个方面均分为高偏倚 间的异质性,采用 I 检验衡量异质性的大小,若各研究
2
[7]
风险、低偏倚风险和不清楚 。采用纽卡斯尔-渥太华量 间无统计学异质性(P>0.1,I <50%),采用固定效应模
2
表(the Newcastle-Ottawa scale,NOS)对纳入的队列研究 型进行分析;反之,则采用随机效应模型进行分析。检
和病例对照研究进行质量评价,包括研究对象选择(0~ 验水准α=0.05。
4 分)、组间可比性(0~2 分)、结果/暴露因素测量(0~3 2 结果
分);1~4分为低质量,5~7分为中等质量,8~9分为高 2.1 文献检索结果与纳入研究基本信息
质量 [8 - 9] 。采用加拿大卫生经济学研究所(Institute of
初检共获得相关文献160篇,经阅读题目、摘要和全
Health Economics,IHE)发布的 IHE 量表对纳入的病例
文后,最终纳入文献 13 篇 [12-24] ,包括病例系列 7 篇 [12-18] 、
系列和病例报道进行质量评价,包括研究目的、研究人
病例报告6篇 [19-24] ,共计203例患者;其中无对照二分类
群、干预方式、结局指标测量、统计学方法、结论与讨论、
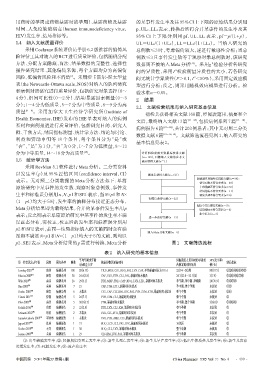
数据文献6篇 [12-16,18] 。文献筛选流程见图1,纳入研究的
利益和资助申明等 18 个条目,每个条目分为“是”或
基本信息见表2。
“否”,“是”为 1 分,“否”为 0 分,1~7 分为低质量,8~13
分为中等质量,14~18分为高质量 。 计算机检索相关数据库获得文献
[10]
(n=159),回溯纳入文献的参考文
1.5 统计学方法 献后获得文献(n=1)
采用RevMan 5.1软件进行Meta分析。二分类资料
以发生率(p)及 95%置信区间(confidence interval,CI) 剔重后获得文献(n=121)
表示。无对照二分类数据的 Meta 分析方法如下:单篇 阅读题目和摘要后排除文献(n=99):
研究对象不符合要求(n=49)
原始研究中某事件的发生数、观察对象总例数、事件发 干预措施不符合要求(n=33)
结局指标不符合要求(n=11)
生率和标准误分别用n、N、p1和SE1表示,当N×p1和N× 研究类型不符合要求(n=6)
初筛后获得文献(n=22)
(1-p1)均大于5时,发生率的抽样分布接近正态分布,
阅读全文后排除文献(n=9):
Meta分析结果即为最终结果,合并的某事件发生率用p 结局指标不符合要求(n=6)
表示;反之则表示单篇原始研究中某事件的发生率不满 非中英文(n=3)
进一步获得文献(n=13)
足正态分布,需校正,校正后的发生率和标准误分别用
p2和SE2表示,若同一结局指标纳入的文献同时含有满
纳入Meta分析文献(n=6)
足和不满足N×p1和N×(1-p1)均大于5的文献,则均以
p2、SE2表示,Meta分析结果的p需进行转换,Meta分析 图1 文献筛选流程
表2 纳入研究的基本信息
平均年龄或年龄 妊娠期妇女用药时的孕周或 HIV发生率/
第一作者及发表年份 国家 研究类型 例数 暴露药物及暴露时间 结局指标
(标准差)/岁 药物暴露时的孕周 例(%)
Loveday 2021 [12] 南非 病例系列 108 28(6.13) TRD、MXF、CFZ、BDQ、PAS、LVX、CAP,平均暴露时长为118 d 22(14~28)周 88(81.5) ①②③④⑤⑥⑦⑧
Palacios 2009 [13] 秘鲁 病例系列 38 24.4(5.8) CAP、LVX、ETH、CLS、PAS,暴露时间未提及 24.7(22.4~32.1)周 3(7.9) ①②③④⑤⑦⑧
Walt 2020 [14] 南非 病例系列 26 29(5.1) ETH、MXF、TRD、CAP、BDQ、LVX、LZD,暴露时间未提及 孕早期、孕中期、孕晚期 20(76.9) ①②⑦⑧
Shin 2003 [15] 美国 病例系列 7 21 CAP、STM、ETH,暴露时间未提及 孕中期、整个孕期 未提及 ①②
Drobac 2005 [16] 秘鲁 病例系列 6 未提及 CFZ、CAP、CLS、KM、LVX、PAS、PTH、STM、ETH,暴露时间未提及 整个孕期 未提及 ①⑥
Tabarsi 2011 [17] 伊朗 病例系列 5 24(7.1) PTH、STM、CLS,暴露时间未提及 整个孕期 未提及 ①
Khan 2007 [18] 南非 病例系列 5 30.8(6.7) STM,暴露时间未提及 孕中期、整个孕期 3(60.0) ①④⑥⑧
Rohilla 2016 [19] 印度 病例报告 2 22(2.8) ETH、LVX、CLS、KM,暴露时间未提及 整个孕期 未提及 ①
Setiawati 2012 [20] 印度 病例报告 2 未提及 LVX、CLS、ETH,暴露时间未提及 整个孕期 未提及 ①
Laniado-Laborín 2018 [21] 墨西哥 病例报告 1 未提及 LVX、PTH、AMK、CLS,暴露时间未提及 整个孕期 未提及 ①
Jaspard 2017 [22] 法国 病例报告 1 31 BDQ、LZD、CLS、PAS、LVX,暴露时间未提及 36周后 未提及 ①
Lhadon 2019 [23] 不丹 病例报告 1 30 BDQ、CLS、LVX,暴露时间未提及 整个孕期 未提及 ①
Lessnau 2003 [24] 美国 病例报告 1 23 CLS、KM、LVX、PAS,暴露时间未提及 整个孕期 未提及 ①
①:出生缺陷发生率;②:妊娠期妇女死亡发生率;③:新生儿死亡发生率;④:新生儿早产发生率;⑤:低出生体质量儿发生率;⑥:新生儿发育
迟缓发生率;⑦:死胎发生率;⑧:流产发生率
中国药房 2022年第33卷第4期 China Pharmacy 2022 Vol. 33 No. 4 ·499 ·