Page 21 - 《中国药房》2021年22期
P. 21
2.2.2 内标溶液 取内标对照品适量,精密称定,加甲 血浆样品,按“2.3”项下方法处理后,再按“2.1”项下条件
醇溶解、稀释,制成质量浓度为50 ng/mL的内标溶液,于 进样分析,记录峰面积。以待测物与内标的峰面积之比
4 ℃下保存,备用。 (y)为纵坐标、待测物的质量浓度(x)为横坐标,采用加
2.3 血浆样品的处理 权最小二乘法(权重为 1/x)进行线性回归,得回归方程
2
取血浆样品 50 µL,置于离心管中,加入内标溶液 为y=0.006 17x+0.001 13(r=0.994 5)。结果显示,芦荟
150 µL,以 2 000 r/min 涡旋 10 min,充分沉淀蛋白,再于 苦素在 1~600 ng/mL 质量浓度范围内与峰面积成良好
4 ℃下以13 000 r/min离心10 min,取上清液置于微量进 的线性关系,定量下限为1 ng/mL。
样管中,进行LC-MS/MS分析。 2.4.3 准确度与精密度试验 取空白血浆,分别加入
2.4 方法学考察 0.1 mg/mL的芦荟苦素贮备液适量,配制成定量下限质
按2020年版《中国药典》(四部)通则“生物样品定量 量浓度(1 ng/mL)和低、中、高质量浓度(3、50、500 ng/mL)
[13]
分析方法验证指导原则”的要求,进行方法学考察 。 的质控血浆样品,按“2.3”项下方法处理后,再按“2.1”项
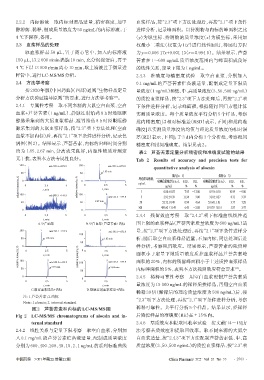
2.4.1 专属性考察 取不同来源的大鼠空白血浆、空白 下条件进样分析,记录峰面积,根据随行回归方程计算
血浆+芦荟苦素(1 ng/mL)、静脉注射给药 8 h 时经眼眶 实测质量浓度。每个质量浓度平行分析5个样品,考察
静脉采集到的大鼠血浆样品、灌胃给药 8 h 时经眼眶静 批内精密度[以相对标准差(RSD)表示,下同]和批内准
脉采集到的大鼠血浆样品,按“2.3”项下方法处理(空白 确度[以实测质量浓度的均值与理论质量浓度的相对误
血浆不加内标)后,再按“2.1”项下条件进样分析,记录色 差(RE)表示,下同];于3 d内分析3个分析批,考察批间
谱图(图2)。结果显示,芦荟苦素、内标的出峰时间分别 精密度和批间准确度。结果见表2。
约为 1.85、2.67 min,分离效果良好,内源性物质对测定 表2 芦荟苦素定量分析精密度和准确度试验的结果
无干扰,表明本方法专属性良好。 Tab 2 Results of accuracy and precision tests for
100 100 1
m/z 393.1→272.9
m/z 393.1→272.9
quantitative analysis of aloesin
1.85 min
50 50 理论质量浓度, 批内(n=5) 批间(n=3)
relative intensity,% 100 0 0 t,min 5 relative intensity,% 100 0 0 t,min 5 ng/mL 实测质量浓度(x±s), RSD, RE, 实测质量浓度(x±s), RSD, RE,
2.5
2.5
%
ng/mL
%
%
%
ng/mL
0.88±0.07
-9.00
0.91±0.10
1
10.99
7.95 -12.00
2
2.91±0.33
3.10±0.27
3.37
4.64
0.94
7.28
50 m/z 555.3→144.9 50 2.67 min m/z 555.3→144.9 50 3 52.32±0.49 11.34 -3.00 53.64±1.81 8.71 3.33
500 489.60±31.49 6.43 -2.08 519.87±30.51 5.87 3.97
0 0
0 2.5 5 0 2.5 5 2.4.4 残留效应考察 取“2.4.2”项下标准曲线线性范
t,min t,min
A.空白血浆 B.空白血浆+芦荟苦素+内标 围上限的血浆样品(芦荟苦素质量浓度为600 ng/mL)适
100 1 m/z 393.1→272.9 1 m/z 393.1→272.9 量,按“2.3”项下方法处理后,再按“2.1”项下条件进样分
100
50 1.85 min 1.85 min 析;随后取空白血浆样品适量,不加内标,同法处理后进
50 样分析,考察残留效应。结果显示,芦荟苦素的残留峰
0
relative intensity,% 100 0 t,min m/z 555.3→144.9 5 relative intensity,% 100 0 0 t,min m/z 555.3→144.9 5 面积小于定量下限质量浓度质控血浆样品芦荟苦素峰
2.5
2.5
2
面积的20%,内标的残留峰面积小于上述质控血浆样品
2
[13]
50 2.67 min 2.68 min 内标峰面积的5%,表明本方法残留效应符合要求 。
50
0 2.4.5 稀释可靠性考察 用空白血浆配制芦荟苦素质
0
0 2.5 5 0 2.5 5
t,min t,min 量浓度为15 000 ng/mL的稀释质控样品,再用空白血浆
C.灌胃血浆样品+内标 D.静脉注射血浆样品+内标
稀释 30 倍(稀释后的理论质量浓度为 500 ng/mL)后,按
注:1.芦荟苦素;2.内标
“2.3”项下方法处理,再按“2.1”项下条件进样分析,考察
Note:1.aloesin;2. internal standard
图2 芦荟苦素和内标的LC-MS/MS图 稀释可靠性。共平行分析5个样品。结果显示,经稀释
Fig 2 LC-MS/MS chromatograms of aloesin and in- 后质控样品的准确度(RE)在±15%内。
ternal standard 2.4.6 基质效应和提取回收率试验 按文献[14-15]方
2.4.2 线性关系与定量下限考察 取空白血浆,分别加 法考察基质效应和提取回收率。取不同来源的大鼠空
入 0.1 mg/mL 的芦荟苦素贮备液适量,配制成质量浓度 白血浆适量,按“2.4.3”项下方法配制芦荟苦素低、中、高
分别为600、400、200、40、10、2、1 ng/mL的系列标准曲线 质量浓度(3、50、500 ng/mL)的质控血浆样品,按“2.3”项
中国药房 2021年第32卷第22期 China Pharmacy 2021 Vol. 32 No. 22 ·2703 ·