Page 30 - 《中国药房》2021年10期
P. 30
下回归方程中计算五味子乙素含量。结果,五味子乙素 质体与洗脱后的脂质体1 mL,加入甲醇9 mL破乳,用微
的平均含量为130.43 μg/mL(RSD=1.91%,n=6),表明 孔滤膜(0.45 μm)滤过,取续滤液。将脂质体溶液与续
本方法重复性良好。 滤液分别注入 HPLC 仪中,分别按照“2.2.1”“2.3.1”项下
12.5 色谱条件测定 2 种成分的峰面积后,代入“2.3.4”项下回
10.0
五味子乙素 归方程中计算药物含量,并计算其包封率:包封率
mV 7.5
U, 5.0 (%)=Na/Nb×100%(式中,Na表示续滤液中药物含量,Nb
2.5 表示脂质体溶液中药物含量)。
0 2.5 脂质体处方工艺的优选
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
t,min 根据实验室经验及文献[16],固定处方量为 5 mL、
A.供试品溶液
磷脂为44 mg、紫杉醇和五味子乙素摩尔比为1 ∶ 5,初步
200
五味子乙素 选定对脂质体制备过程影响相对较大的胆固醇含量
150
mV 100 (A)、紫杉醇含量(B)与探头超声时间间隔(简称“时间间
U,
50 隔”,C)作为考察因素,两药平均包封率(Y,%)作为考察
0 指标,采用Box-Benhken设计-效应面实验优选脂质体的
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
t,min 处方工艺。各因素水平编码见表 2,实验设计方案与结
B.对照品溶液 果见表3,方差分析结果见表4。
60 表2 各因素水平编码
50
40 Tab 2 Factors and levels code
mV 30
U, 20 因素 -1. 0. 1.
10 A(胆固醇),mg 6. 8. 10.
0
B(紫杉醇),mg 0.4 0.6 0.8
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
t,min C(时间间隔),s 3. 4. 5.
C.空白溶液 表3 Box-Behnken实验设计方案与结果
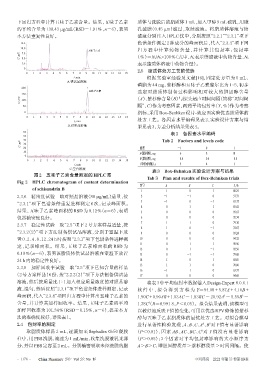
图2 五味子乙素含量测定的HPLC图
Tab 3 Plan and results of Box-Behnken trials
Fig 2 HPLC chromatogram of content determination
序号 A B C Y,%
of schisandrin B
1 1 0 1 80.25
2.3.6 精密度试验 取对照品溶液(80 μg/mL)适量,按 2 -1 -1 0 57.73
3 -1 0 -1 65.37
“2.3.1“项下色谱条件重复进样测定 6 次,记录峰面积。
4 0 -1 1 85.41
结果,五味子乙素峰面积的 RSD 为 0.12%(n=6),表明 5 0 0 0 95.67
仪器精密度良好。 6 0 0 0 92.74
7 1 1 0 79.30
2.3.7 稳定性试验 取“2.5”项下2号方案样品适量,按
8 1 0 -1 72.67
“2.3.2(2)”项下方法制备供试品溶液,分别于室温下放 9 0 0 0 93.24
置0、2、4、8、12、24 h时按照“2.3.1”项下色谱条件进样测 10 0 0 0 94.32
11 0 1 1 90.96
定,记录峰面积。结果,五味子乙素峰面积的 RSD 为
12 0 1 -1 92.56
0.10%(n=6),表明该脂质体供试品溶液在室温下放置 13 0 -1 -1 79.68
24 h内的稳定性良好。 14 -1 0 1 68.85
15 1 -1 0 70.06
2.3.8 加样回收率试验 取“2.5”项下已知含量的样品
16 -1 1 0 63.37
(2 号方案样品)6 份,按“2.2.2(2)”项下方法制备供试品 17 0 0 0 94.45
溶液,然后按质量比1 ∶ 1加入相应质量浓度的对照品溶 将表3中平均包封率数据输入Design-Expert 8.0.6.1
液,混匀,然后按照“2.3.1”项下色谱条件进样测定,记录 软 件 中 ,拟 合 得 到 方 程 为 Y=94.08 + 5.87A + 4.16B +
峰面积,代入“2.3.4”项回归方程中计算出五味子乙素的 1.90C+0.90AB+1.03AC-1.83BC-20.92A -5.55B -
2
2
含量,并计算其加样回收率。结果,五味子乙素的平均 1.38C(R=0.991 8,P<0.05)。拟合结果表明,该模型可
2
加样回收率为101.34%(RSD=0.15%,n=6),提示本方 以较好地反映Y值的变化,可用以优选RPV修饰的紫杉
法的准确度较好,详见表1。 醇与五味子乙素脂质体的最优处方工艺。对拟合模型
2
2
2.4 包封率的测定 进行显著性检验发现,A、B、C、A 、B 对 Y 值有显著影响
取脂质体样品 2 mL,逐滴加至 Sephadex G-50 凝胶 (P<0.01),因素 AB、AC、BC、C 对 Y 值没有显著影响
2
柱中,用PBS洗脱,流速为1 mL/min,收集洗脱液乳光部 (P>0.05);3 个因素对平均包封率影响的大小顺序为
分,并以PBS定容至2 mL。分别精密吸取未经洗脱的脂 A>B>C,即胆固醇质量>紫杉醇质量>时间间隔。使
·1176 · China Pharmacy 2021 Vol. 32 No. 10 中国药房 2021年第32卷第10期