Page 86 - 《中国药房》2021年8期
P. 86
0.10 0.10
贝林司他 贝林司他
0.08 0.08
0.06 0.06
AU AU
0.04 0.04
杂质A 未知 杂质H 杂质D 杂质A 未知
0.02 0.02
0 0
0 5 10 15 20 25 30 35 40 45 50 55 60 0 5 10 15 20 25 30 35 40 45 50 55 60
t,min t,min
A.未破坏供试品溶液 B.高温破坏供试品溶液
0.10 0.10
贝林司他 贝林司他
0.08 0.08
0.06 0.06 杂质D
AU AU
0.04 0.04
杂质H 杂质D 杂质A 未知 未知
0.02 0.02 杂质A
0 0
0 5 10 15 20 25 30 35 40 45 50 55 60 0 5 10 15 20 25 30 35 40 45 50 55 60
t,min t,min
C.光照破坏供试品溶液 D.酸破坏供试品溶液
0.10 0.10
贝林司他 杂质D 溶剂峰
0.08 0.08 贝林司他
0.06 0.06
AU 未知 AU
0.04 0.04
0.02 未知 杂质A 0.02 杂质D 杂质A
未知 未知 杂质H 杂质G 杂质C 未知 杂质H 未知
0 0
0 5 10 15 20 25 30 35 40 45 50 55 60 0 5 10 15 20 25 30 35 40 45 50 55 60
t,min t,min
E.碱破坏供试品溶液 F.氧化破坏供试品溶液
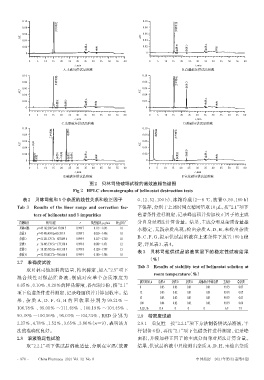
图2 贝林司他破坏试验的高效液相色谱图
Fig 2 HPLC chromatographs of belinostat destruction tests
表2 贝林司他和5个杂质的线性关系和校正因子 0、12、52、100 h)、冰箱冷藏(2~8 ℃,放置 0、50、100 h)
Tab 3 Results of the liner range and correction fac- 下保存,分别于上述时间点精密量取10 μL,按“2.1”项下
tors of belinostat and 5 impurities 色谱条件进样测定,记录峰面积并按加校正因子的主成
待测成分 回归方程 r 线性范围,μg/mL 校正因子 分自身对照法计算含量。结果,主成分和总杂质含量基
贝林司他 y=45 162.380 5x+117.094 5 0.999 7 0.113~1.693 1.0 本稳定,无新杂质出现;检出杂质 A、D、H,未检出杂质
杂质A y=47 496.424 0x+85.391 9 0.999 7 0.050~1.496 1.0
杂质D y=51 251.575 7x-887.889 6 0.999 9 0.117~1.750 1.0 B、C、F、G,提示供试品溶液在上述条件下放置 100 h 稳
杂质F y=36 443.339 5x-173.330 4 0.999 8 0.098~1.471 1.2 定,详见表3、表4。
杂质G y=30 505.785 0x-401.318 9 0.999 8 0.120~1.799 1.5 表 3 贝林司他供试品溶液常温下的稳定性试验结果
杂质H y=52 330.412 7x-596.644 0 0.999 9 0.100~1.506 1.0
(%%)
2.7 准确度试验
Tab 3 Results of stability test of belinostat solution at
取贝林司他原料药适量,精密称定,加入“2.5”项下
room temperature(%%)
混合线性对照品贮备液,制成对应单个杂质浓度为
放置时间,h 杂质A 杂质D 杂质H 其他最大单体杂质 主成分 总杂质
0.05%、0.10%、0.20%的样品溶液,各配制 3 份,按“2.1” 0 0.03 0.02 0.01 0.01 99.93 0.07
项下色谱条件进样测定,记录峰面积并计算回收率。结 12 0.03 0.02 0.01 0.01 99.93 0.07
52 0.03 0.02 0.01 0.01 99.92 0.07
果 ,杂 质 A、D、F、G、H 的 回 收 率 分 别 为 99.21% ~
100 0.04 0.02 0.01 0.01 99.93 0.08
106.78% 、95.01% ~111.48% 、100.19% ~104.45% 、 RSD,% 15.4 0 0 0 6.9 7.9
90.18% ~100.56% 、95.03% ~104.33% ,RSD 分 别 为 2.9 精密度试验
2.37%、4.78%、1.52%、3.65%、3.86%(n=9),表明该方 2.9.1 重复性 按“2.2.1”项下方法制备供试品溶液,平
法的准确度良好。 行制备 6 份,再按“2.1”项下色谱条件进样测定,记录峰
2.8 溶液稳定性试验 面积,并按加样正因子的主成分自身对照法计算含量。
取“2.2.1”项下供试品溶液适量,分别在室温(放置 结果,供试品溶液中只检测出杂质A、D、H,未检出杂质
·976 · China Pharmacy 2021 Vol. 32 No. 8 中国药房 2021年第32卷第8期