Page 131 - 202018
P. 131
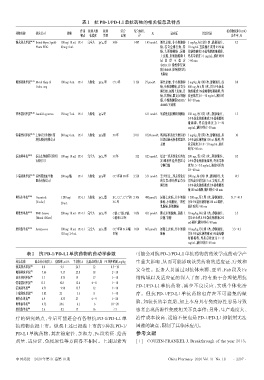
表1 抗PD-1/PD-L1单抗药物的相关信息及特点
作用 抗体人源 抗体 结合 结合面积, 抗药物抗体(ADA)
药物名称 研发公司 规格 Kd 适应证 用法用量
靶点 化程度 类型 区域 Å 2 发生率,%
纳武利尤单抗 [24,34] Bristol-Myers Squibb 100 mg∶10 mL PD-1 完全人 IgG4κ型 N环 1 487 1.45 nmol/L 黑色素瘤,非小细胞肺 3 mg/kg,每2周1次,静脉滴注, 8.5
Pharm EEIG 40 mg∶4 mL 癌,霍奇金淋巴瘤,肾 10 mg/mL直接输注或用0.9%氯
癌,头颈部鳞癌 ,尿路 化钠溶液或5%葡萄糖溶液稀释,
上皮癌,肝细胞癌微卫 终质量浓度≥1 mg/mL,滴注时间
星 高 度 不 稳 定 >60 min
(MSI-H)/ 错配修复缺
陷(dMMR)的转移性结
直肠癌
帕博利珠单抗 [25,35] Merck Sharp & 100 mg∶4 mL PD-1 人源化 IgG4κ型 C′D环 2 126 27 pmol/L 黑色素瘤,非小细胞肺 2 mg/kg,每3周1次,静脉滴注,或 0.8
Dohm corp 癌,头颈部鳞癌,霍奇金 400 mg,每6周1次,用0.9%氯化
淋巴瘤,尿路上皮癌,胃 钠溶液或5%葡萄糖溶液稀释,终
癌,宫颈癌,默克尔细胞 质量浓度为1~10 mg/mL,滴注时
癌,小细胞肺癌MSI-H/ 间>30 min
dMMR实体瘤
西米普利单抗 [28,36] Sanofi-Regeneron 350 mg∶7 mL PD-1 人源化 IgG4型 6.11 nmol/L 转移性皮肤鳞状细胞癌 350 mg,每 3 周 1 次,静脉滴注, 1.3
0.9%氯化钠溶液或5%葡萄糖溶
液 稀 释 ,终 质 量 浓 度 为 1~20
mg/mL,滴注时间>30 min
特瑞普利单抗 [29,37] 上海君实生物医药 240 mg∶6 mL PD-1 人源化 IgG4型 FG环 2 011 0.324 nmol/L 既往标准治疗失败后的 3 mg/kg,每2周1次,静脉滴注,用 18
科技股份有限公司 局部进展或转移性黑色 0.9%氯化钠溶液100 mL稀释,终
素瘤 质量浓度为1.0~3.0 mg/mL,滴注
时间>60 min
信迪利单抗 [30,38] 信达生物制药(苏州) 100 mg∶10 mL PD-1 完全人 IgG4κ型 FG环 322 0.25 nmol/L 经过二线系统化疗的复 200 mg,每 3 周 1 次,静脉滴注, 0.5
有限公司 发/难治性经典型霍奇 0.9%氯化钠溶液稀释,终质量浓
金淋巴瘤 度为1.5~5.0 mg/mL,滴注时间为
30~60 min
卡瑞利珠单抗 [31,39] 苏州盛迪亚生物 200 mg/瓶 PD-1 人源化 IgG4型 CC′环和 FG环 2 520 3.31 nmol/L 至少经过二线系统化疗 200 mg,每2周1次,静脉滴注,先 14.5
医药有限公司 的复发/难治性霍奇金 用灭菌注射用水5 mL复溶后,用
淋巴瘤 0.9%氯化钠溶液或5%葡萄糖溶
液100 mL稀释,滴注时间>60 min
阿特朱单抗 [32,40] Genentech 1 200 mg∶ PD-L1 人源化 IgG1κ型 BC、CC′、C′C″和 2 106 400 pmol/L 尿路上皮癌,非小细胞 1 200 mg,每3周1次,静脉滴注, 31.7~41.9
(Roche) 20 mL FG 环 肺癌,小细胞癌,三阴性 用0.9%氯化钠溶液250 mL稀释,
乳腺癌,肝细胞癌 滴注时间≥60 min
阿维鲁单抗 [22,41] EMD Serono 200 mg∶10 mL PD-L1 完全人 IgG1λ型 C链、C′链、F链、 1 856 42.1 pmol/L 默克尔细胞癌,尿路上 10 mg/kg,每2周1次,静脉滴注, 3.5
(Merck /Pfizer) G链和CC'环 皮癌,肾癌 用0.45%或0.9%氯化钠溶液250
mL稀释,滴注时间≥60 min
度伐鲁单抗 [33,42] AstraZeneca 500 mg∶10 mL PD-L1 完全人 IgG1κ型 CC′环和 N 末端 1 624 667 pmol/L 尿路上皮癌,非小细胞 10 mg/kg,每2周1次,静脉滴注, 3.3~4.3
120 mg∶2.4 mL 区域 肺癌 用0.9%氯化钠溶液或5%葡萄糖
溶液稀释,终质量浓度为 1~15
mg/mL,滴注时间≥60 min
表2 抗PD-1/PD-L1单抗药物的药动学参数 可能会对抗PD-1/PD-L1单抗药物的药效学或药动学产
药品名称 稳态分布容积,L 清除率,mL/h 半衰期,d 达稳态时间,周 PK线性范围,mg/kg 生重大影响,从而可能影响该类药物的适应证、疗效和
纳武利尤单抗 [36] 8.0 9.5 26.7 12 0.3~10 安全性。医务人员通过对抗体来源、亚型、Fab 段及 Fc
帕博利珠单抗 [37] 7.66 9.17 25.8 18 2~10
西米普利单抗 [38] 5.3 8.75 19. 17 1~10 结构域以及适应证的深入了解,将有助于合理使用抗
特瑞普利单抗 [39] 13.3 10.8 12.6 6~8 1~10 PD-1/PD-L1 单抗药物,减少不良反应,实现个体化治
信迪利单抗 [40] 4.71 9.98 13.7 12 1~10
卡瑞利珠单抗 [41] 3.82 22. 5.5 8 1~10 疗。但抗 PD-1/PD-L1 单抗药物也存在不可避免的缺
阿特朱单抗 [42] 6.9 8.33 27. 6~9 1~20 陷,如较长的半衰期,加上本身具有免疫原性容易导致
阿维鲁单抗 [43] 4.72 24.6 6.1 6 10~20
度伐鲁单抗 [44] 5.6 8.2 17. 16 ≥3 患者出现药源性免疫相关不良事件;另外,生产难度大、
疗的研究热点,今后可能还会有各种抗 PD-1/PD-L1 单 治疗成本较高、运输不便也是 PD-1/PD-L1 抑制剂无法
抗药物获批上市。纵观上述已批准上市的 9 种抗 PD-1/ 回避的缺点,限制了其临床应用。
PD-L1 单抗药物,其在稳定性、亲和力、Fc 段特征、给药 参考文献
剂量、适应证、免疫原性等方面各不相同。上述因素均 [ 1 ] COUZIN-FRANKEL J. Breakthrough of the year 2013:
中国药房 2020年第31卷第18期 China Pharmacy 2020 Vol. 31 No. 18 ·2297 ·