Page 135 - 《中国药房》2022年13期
P. 135
本文从聚合物前药递送系统、缺氧型前药递送系统等方 (DMSA-Fe3O4 )磁性纳米颗粒与硼替佐米(BTZ)和 GA
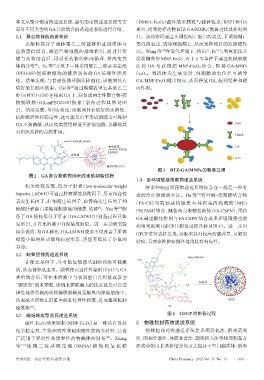
面对不同类型的GA共价结合前药递送系统进行介绍。 聚合,得到化疗药物BTZ-GA/MNPs(制备过程具体见图
1.1 聚合物前药递送系统 3)。该药物可通过上调促凋亡蛋白的表达,下调抑凋亡
水溶性高分子载体聚乙二醇能够阻止脂质体与 蛋白的表达,诱导细胞凋亡,从而发挥较好的抗肿瘤作
[14]
2+
3+
血清蛋白结合,减轻巨噬细胞的摄取作用,通过共价 用。Wang等 在氮气环境下,将Fe 、Fe 与氢氧化铵共
键与药物结合后,可延长药物的体内循环,并改变其 沉淀制备得 MNP-Fe3O4,再于 4 ℃条件下通过机械吸收
[7]
[6]
体内分布 。Yu等 开发了一种采用聚乙二醇-β-谷甾醇 法 将 GA 与 获 得 的 MNP-Fe3O4 结 合 ,即 得 GA-MNP-
(PEG-SS)偶联物修饰的磷脂制备的 GA 长循环脂质 Fe3O4。当机体发生病变时,细胞膜的电位差可诱导
体。结果发现,与普通长循环脂质体相比,该制剂具有 GA-MNP-Fe3O4做出响应,从而释放 GA,起到缓释和靶
更好的长循环效果。Cai 等 通过酯键将甲氧基聚乙二 向作用。
[8]
醇(mPEG)-2000连接到GA上,制备成两亲性聚合物-药
物偶联物(GA-mPEG2000)胶束(制备过程具体见图
2)。结果发现,与 GA 相比,该制剂具有更好的水溶性、
抗肿瘤活性和稳定性,这可能是由于形成的胶束可保护
GA不被酶解,从而使其缓慢释放至肿瘤细胞,并降低其 Fe3O4
对组织器官的毒副作用。
DMSA
mPEG-2000或LMWH
亲水性壳 GA
(mPEG-2000或
LMWH)
自组装
BTZ
疏水性核(GA)
图3 BTZ-GA/MNPs的制备过程
图2 GA聚合物前药纳米胶束的制备过程
1.4 多环境敏感型前药递送系统
相关研究发现,低分子肝素(low-molecular weight 将多种响应型药物递送系统结合在一起是一种有
heparin,LMWH)可通过肿瘤源性黏附因子、肝素结合性 效的治疗肿瘤的方法。Du 等 将叶酸-壳聚糖结合物
[15]
表皮生长因子、肝细胞生长因子、血管内皮生长因子和 (FA-CS)与端氨基热敏聚 N-异丙基丙烯酰胺(NH2-
[9]
[10]
硫酸肝素蛋白多糖抑制肿瘤的侵袭、转移 。Yan等 制 PNIPAM)络合,制备出壳聚糖接枝体(FA-CSPN),再将
备了 GA 接枝低分子肝素(GA-LMWH)(制备过程具体
GA 通过酯化作用与 FA-CSPN 结合成多环境敏感型前
见图2),并在水溶液中自组装成胶束。进一步动物实验 药纳米胶束(GFCP)(制备过程具体见图 4)。进一步对
结果表明,与GA相比,GA-LMWH胶束不仅改善了肝癌
GFCP进行表征发现,该胶束具有较高的载药量,可靶向
模型小鼠的肝功能和病理形态,还显著延长了小鼠的
肿瘤,且对多种肿瘤微环境均具有响应性。
寿命。
1.2 缺氧型前药递送系统
GA NH2-PNIPAM
在缺氧条件下,具有缺氧敏感基团的药物可被激
活,从而被释放出来。缺氧靶向近红外染料(Cy7)与GA
共价结合后,可在水溶液中与表面蛋白自组装成新型
自组装
“镶嵌型”纳米颗粒,该纳米颗粒最大的优点就是可以选 CS
择性地将负载的药物偶联物释放至缺氧的肿瘤细胞中,
从而减少药物在肝脏中的非特异性积聚,进而提高抗肿 GFCP
瘤效果 。 FA
[11]
1.3 磁场响应型前药递送系统 图4 GFCP的制备过程
磁性 Fe3O4纳米颗粒(MNP-Fe3O4 )是一种具有良好 2 物理包封药物递送系统
化学稳定性、生物相容性和超顺磁性的纳米材料,已被 物理包封药物递送系统是采用乳化法、溶剂蒸发
广泛用于靶向性和缓释性药物载体的制备 。Zhang 法、固相分散法、薄膜水合法、脂质插入法等物理制备方
[12]
等 [13] 使 用 二 巯 基 琥 珀 酸(DMSA)修 饰 的 氧 化 铁 法将药物以非共价结合的方式包封于空白脂质体、纳米
中国药房 2022年第33卷第13期 China Pharmacy 2022 Vol. 33 No. 13 ·1661 ·